La soluzione tampone è solitamente una miscela di un acido debole e il sale di quell'acido, o una base debole e il sale di quella base. Questa soluzione ha lo scopo di prevenire il verificarsi di variazioni molto grandi nel pH o pOH di una soluzione.
Di seguito sono riportati alcuni esempi di soluzioni tampone:
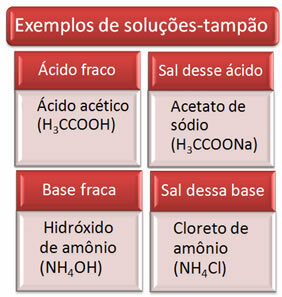
L'efficacia della soluzione tampone è visibile nel nostro sangue, dove, anche con l'aggiunta di acido o base in piccole quantità al plasma sanguigno, non vi è praticamente alcuna variazione del suo pH.
Come avviene questo, visto che se all'acqua aggiungiamo acidi o basi, il suo pH cambia velocemente?
Il sangue umano è un sistema tampone leggermente basico, cioè è un liquido tamponato: il suo pH rimane costante tra 7,35 e 7,45. Uno dei tamponi più interessanti e importanti nel sangue è formato dall'acido carbonico (H2CO3) e dal sale di questo acido, bicarbonato di sodio (NaHCO3).
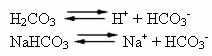
Pertanto, ci sono le seguenti specie in questa soluzione tampone:
H2CO3: presente in grandi quantità, essendo un acido debole, soffre poca ionizzazione;
H+: dalla ionizzazione di H2CO3;
HCO3-: presente anche in quantità elevate, dalla ionizzazione di H2CO3 e dissociazione salina (NaHCO3);
A+: dalla ionizzazione di NaHCO3;
Se a questa soluzione viene aggiunta una piccola concentrazione di acido, si verificherà la sua ionizzazione, generando cationi H+, che reagirà con gli anioni HCO3- presente nel terreno, originando acido carbonico non ionizzato. Non c'è variazione di pH.
Se viene aggiunta una base, verranno generati anioni OH-. Questi ioni si combinano con i cationi H+, dalla ionizzazione di H2CO3. Quindi, gli anioni OH- vengono neutralizzati, mantenendo il pH del mezzo.
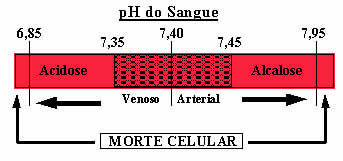
Oltre a questa soluzione tampone citata, ne esistono anche altre due presenti nel sangue, che sono: H2POLVERE4/HPO42- e alcune proteine. Se non ci fossero tali soluzioni tampone nel sangue, l'intervallo di pH potrebbe essere seriamente distorto. Se il pH del sangue sale sopra 7,8, si parla di alcalosi. Se il pH scende troppo, al di sotto di 6,8, sarà uno stato di acidosi. Entrambe sono condizioni pericolose che possono portare alla morte.
di Jennifer Fogaça
Laureato in Chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/solucaotampao-no-sangue-humano.htm


