Come spiegato nel testo Reazioni di addizione, queste reazioni organiche di solito si verificano con composti che hanno insaturazione (doppi legami o triple), in cui il legame pi greco è rotto, consentendo l'ingresso di atomi o gruppi di atomi nella catena. carbonico.
Tuttavia, questo tipo di reazione si verifica anche nel caso di cicloalcani (idrocarburi a catena chiusa con solo legami saturi (semplici) tra i carboni) che hanno tre o quattro atomi di carbonio. Notare un esempio di seguito, che è la bromurazione (reazione di alogenazione) del ciclopropano:
CH2
/ \ + fratello2 → fratello CH2 CH2 CH2 ─ fratello
H2C CH2
Allo stesso modo, c'è anche la reazione di addizione chiamata idroalogenazione o aggiunta di alogenuro, come mostrato di seguito:
CH2
/ \ + HBr → H CH2 CH2 CH2 ─ fratello
H2C CH2
Si noti che, in entrambi i casi, la molecola è stata rotta e sono stati prodotti composti a catena aperta.
Ma ciò non avviene altrettanto facilmente nei cicloalcani con cinque o più atomi di carbonio. D'altra parte, questi composti hanno maggiori probabilità di funzionare
reazioni di sostituzione, in cui non si rompe il legame, ma si sostituiscono uno o più atomi di idrogeno legati al carbonio con atomi di altri elementi.Il ciclopentano può ancora effettuare reazioni di addizione, ma solo a temperature più elevate (circa 300°C). Nel caso del cicloesano, questo è molto difficile. Ciò che effettivamente fa sono reazioni di sostituzione, come la seguente clorazione:
CH2 CH2
/ \ / \
H2C CH2 H2C CH Cl
│ │ + Cl2→ │ │ + HCl
H2C CH2 H2C CH2
\ / \ /
CH2 CH2
Gli anelli con cinque o più atomi di carbonio non reagiscono con gli acidi idroalici, come l'HBr, in aggiunta alle reazioni.
Ma perché succede questo? Perché i cicloalcani a tre o quattro atomi di carbonio effettuano reazioni di addizione e i cicloalcani con più atomi di carbonio tendono a non farlo?
Bene, questo perché il ciclopropano e il ciclobutano sono più instabili, quindi è più facile rompere i loro legami.
Johann Friedrich Adolf von Bayer (1835-1917)
Per spiegarlo, il chimico tedesco Johann Friedrich Adolf von Bayer (1835-1917) sviluppò, nel 1885, il cosiddetto Teoria dello stress anulare, che ha dimostrato che i quattro legami formati dagli atomi di carbonio sarebbero più stabili quando avessero un angolo pari a 109º 28', come nel caso del seguente metano:

I quattro singoli legami del metano hanno un angolo di 109º 28'
Questo è l'angolo più stabile perché corrisponde alla massima distanza possibile tra gli atomi in una geometria tetraedrica. Con questo, la repulsione elettronica (repulsione tra gli elettroni negli strati di valenza degli atomi) si riduce.
I cicloalcani con tre, quattro e cinque atomi di carbonio hanno angoli di legame tra i atomi di carbonio inferiori a 109º 28'. Guarda:
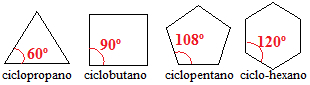
Angoli dei legami cicloalcani
Sulla base di questi angoli reali, che possiamo chiamare genericamente α, il calcolo della tensione di legame può essere effettuato utilizzando la seguente formula:
tensione = 109º 28' - α
2
Sappiamo che il ciclopropano è il cicloalcano più instabile e anche più reattivo, e questo è confermato calcolando la tensione del suo anello rispetto agli altri:
tensione ciclopropano = 109º 28' – 60º = 109º – 60º + 28' = 49º + 28' = 24,5º + 14
2 2 2
Poiché 0,5º = 30, allora abbiamo:
tensione ciclopropano = 24º + 30' + 14' = 24º 44'
ciclobutano tensione = 109º 28' – 90º = 9º 44'2
tensione ciclopentano = 109º 28' – 108º = 0º 44'2
Secondo la teoria delle tensioni di Bayer, maggiore è questa tensione, più instabile sarà il ciclano, cioè maggiore sarà la differenza tra l'angolo reale (α) e l'angolo teorico (109º 28'), più instabile e, di conseguenza, più reattivo sarà il sostanza.
Ecco perché il ciclopropano è il meno stabile dei cicloalcani.
Tuttavia, c'era un errore nella teoria di Bayer, perché se continuiamo a fare questo calcolo dello stress per il cicloesano, dove l'angolo di connessione è 120°, vedremo che il valore sarà anche minore di quello del ciclopropano, dando pari a -5° 16'. Ciò indicherebbe il fatto che il cicloesano dovrebbe essere ancora più instabile e svolgere reazioni di addizione, il che non è il caso in pratica.
La spiegazione di questo fatto fu trovata, nel 1890, dal chimico tedesco Hermann Sachse e dimostrata, nel 1918, dal chimico anche tedesco Ernst Mohr. Secondo questi scienziati, l'errore nella teoria dello stress anulare di Bayer risiederebbe nel fatto che egli considerava che tutti i cicloalcani sono complanari, cioè tutti i loro atomi di carbonio sono in un unico piano, com i disegni delle loro strutture mostrati sopra.
Tuttavia, in realtà, gli anelli dei cicloalcani con più di cinque atomi di carbonio non sono piatti, ma i loro atomi. acquisire conformazioni spaziali che annullano le tensioni tra le connessioni, stabilendo un angolo di 109º 28' tra le Connessioni.
Ad esempio, guarda il caso del cicloesano. Non è, infatti, piatto con un angolo di 120° tra i suoi legami, ma, di fatto, i suoi atomi "ruotano", formando due possibili conformazioni, la conformazione a "sedia" e la conformazione a "barca":
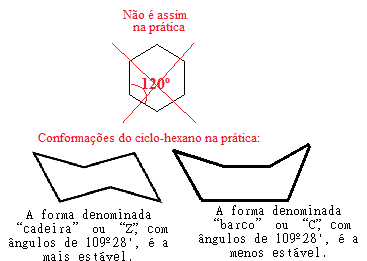
Possibili conformazioni del cicloesano in pratica
Si noti che, poiché l'angolo reale del cicloesano è uguale a 109º 28', è un composto molto stabile, quindi la sua molecola non si rompe, non partecipando quindi alle reazioni di addizione. Si noti inoltre che la forma "a sedia" è la più stabile, essendo quella che predomina sempre nelle miscele, questo perché, in questa conformazione, gli atomi di idrogeno legati al carbonio sono più distanti tra loro. altri.
di Jennifer Fogaça
Laureato in Chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/teoria-das-tensoes-dos-aneis-bayer.htm

