IL nihonium, numero atomico 113 e simbolo Nh, è un elemento chimico appartenente al gruppo 13 della Tavola Periodica. Inoltre, è un elemento super pesante che non si trova in natura. Pertanto, il suo ottenimento può essere fatto solo artificialmente, attraverso reazioni di fusione nucleare. Le caratteristiche chimiche del nihonium non sono ancora così chiare, ma si ipotizza che si comporti in modo simile alla sua controparte più leggera, il tallio, in alcuni casi.
Il nionio è stato inizialmente ottenuto per fusione 70Zn con il 209Bi, al Riken Institute, Giappone, nel 2003. Sebbene anche scienziati russi e americani abbiano chiesto di essere riconosciuti come scopritori dell'elemento 113, la IUPAC ha riconosciuto gli scienziati giapponesi. Il nome si riferisce alla parola Nihon, come i giapponesi chiamano il loro paese natale.
Leggi anche: Gallio — un altro elemento chimico appartenente al gruppo 13 della tavola periodica
riassunto sul nihonium
È un elemento chimico sintetico situato nel gruppo 13 del Tavola periodica.
La sua produzione è iniziata nel 2003, presso il Riken Institute, in Giappone.
Costituisce il gruppo di elementi più recentemente inseriti nella Tavola Periodica, nel 2015.
I suoi studi sono ancora molto recenti, ma alcuni cercano di collegarlo ad altri elementi del gruppo 13, come il tallio.
La sua produzione è Fusione nucleare, utilizzando gli isotopi di 70Zn e atomi di 209Bi.
Proprietà del nionio
Simbolo: no
Numero atomico: 113
Massa atomica: tra il 278 e il 286 c.u. (non ufficiale da Iupac)
Configurazione elettronica: [Rn] 7s2 5f14 6d10 7p1
Isotopo più stabile:286Nh (9,5 secondi di metà vita, che può aumentare di 6,3 secondi o diminuire di 2,7 secondi)
Serie chimica: gruppo 13, elementi super pesanti
caratteristiche del nihonium
Nihonium, simbolo Nh e numero atomico 113, era uno degli ultimi elementi inclusi nella Tavola Periodica. La sua ufficializzazione è avvenuta il 30 dicembre 2015 dall'Unione internazionale di chimica pura e applicata (IUPAC), mentre il suo nome è stato ufficializzato solo a metà del 2016.
Gli elementi in questa regione della tavola periodica sono altamente instabili, il che significa che non possono essere trovati in natura. Pertanto, a fronte di una presunta esistenza, subirebbero quasi istantaneamente un decadimento radioattivo - l'emissione di particelle nucleari, come α e β - al fine di ottenere una maggiore stabilità.
Tuttavia, quando emettono particelle nucleari, finiscono per subire una trasmutazione nucleare, cioè diventano un nuovo elemento chimico. Pertanto, gli elementi superpesanti, come Nh, devono essere prodotti in laboratorio, il che lo rende a elemento chimico sintetico.
Nh, come altri elementi superpesanti, è influenzato da effetti relativistici — in modo semplice, le distanze da ciò che si osserva a ciò che ci si aspetta, per relatività. Pertanto, studi matematici in campo teorico, che simulano le conseguenze dell'effetto relativistico, hanno evidenziato quel nihonium potrebbe interagire debolmente con il quarzo, ma avere buon assorbimento a oro, come la sua controparte più leggera, il tallio (Tl).
Studi teorici preliminari hanno indicato anche il volatilità da Nh. Per quanto riguarda l'adsorbimento al quarzo, il tallio forma prontamente TlOH, per esempio, e si sospetta che il nihonium faccia lo stesso.
Anche così, come gli studi sono ancora molto preliminari e recenti, gran parte di ciò che è stato prodotto è oggetto di discussione ed è difficile determinare con precisione le proprietà fisico-chimiche del nihonium.
Ottenere il Nihonium
L'elemento 113, fino ad oggi, è stato ottenuto in due modi: tramite reazioni di fusione fredda, con la fusione dello zinco (Zn, Z = 30) con il bismuto (Bi, Z = 83), e anche attraverso il decadimento alfa dell'elemento 115.
Nel primo esempio, il zinco è accelerato al 10% del velocità della luce, al fine di vincere le forze repulsive dei due nuclei. Viene quindi prodotto un isotopo 279Nh, che finisce per emettere un neutrone e produrre il 278Nh.

Con un'emivita di circa 34 millisecondi, l'isotopo 278Nh subisce sei decadimenti alfa (emissioni di particelle alfa) nell'elemento mendelevio (Md).
Nel secondo caso, l'elemento 113 deriva dal decadimento alfa dell'elemento 115 (ora noto come muscovio) dopo che è stato sintetizzato. Un modo è la reazione di fusione a caldo degli ioni 48Ca con isotopi 243ah, producendo il 288Mc e poi, per decadimento alfa, il 284Nh, che continua a subire il decadimento alfa.
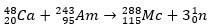
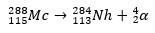
Vedi anche: Hassium — l'elemento chimico sintetico più pesante di cui si analizzano le proprietà
storia del nihonium
Le ricerche dell'elemento 113 sono iniziate nel 2003. I ricercatori giapponesi del Riken Institute hanno accelerato gli isotopi di 70Zn al 10% della velocità della luce per entrare in collisione con il 209Bi, attraverso una reazione di fusione. Così, sono riusciti a produrre quello che ora conosciamo come 278Nh.
Tuttavia, è stato solo nel 2012 che I ricercatori giapponesi sono stati in grado di rilevare la serie completa di decadimento alfa dell'elemento 113, contattando la IUPAC per rivendicare la scoperta.
In concomitanza con gli sforzi giapponesi, gli scienziati russi guidati da Yuri Oganessian, in collaborazione con Scienziati americani arrivarono anche a identificare l'elemento 113 attraverso i decadimenti alfa dell'elemento 115. Tali esperimenti mettono anche scienziati russi e americani in lizza per il riconoscimento dell'elemento 113.

Tuttavia, la IUPAC ha ritenuto che le prove dell'istituto Riken fossero più solide, consentendo così ai giapponesi di avere il diritto di nominare l'elemento 113. Il nome scelto era nihônio, simbolo Nh, in riferimento al paese Giappone. La parola Giappone è scritta dai giapponesi utilizzando due caratteri cinesi che significano "terra del sole nascente" e vengono letti come Nihon o Nippon.
Il nome nihonium fu scelto anche perché, nel 1908, il chimico giapponese Masataka Ogawa pubblicò che aveva scoperto l'elemento 43, nominandolo giapponese, simbolo Np (che oggi appartiene al nettunio, Z = 93). Tuttavia, in seguito, è stato dimostrato che l'elemento 43 era instabile, non essendo presente in natura e sintetizzato solo nel 1937, ricevendo il nome di tecnezio (Tc).
Così, il giapponese è scomparso dalla tavola periodica. Tuttavia, anni dopo, fu dimostrato che, in effetti, Ogawa aveva scoperto l'elemento 75 (ora noto come renio). Tuttavia, a quel tempo, l'elemento renio era già stato ufficialmente scoperto nel 1925 e battezzato.
Risolti esercizi su nihonium
domanda 1
Il nionio, simbolo Nh e numero atomico 113, è un elemento chimico introvabile in natura a causa della sua breve emivita. Il più duraturo di loro, il 286Nh, ha circa 9,5 secondi. Sapendo che l'emivita è il tempo necessario affinché la quantità della specie si dimezzi, quanti secondi sono necessari affinché la quantità dell'isotopo di cui sopra sia 1/16 della quantità iniziale?
A) 9.5
B) 19
C) 28.5
D) 38
E) 47.5
Risoluzione:
Alternativa D
Ogni 9,5 secondi, la quantità dell'isotopo diminuisce della metà. Quindi, dopo 9,5 secondi, il suo importo è la metà dell'importo iniziale. Altri 9,5 secondi, per un totale di 19 secondi, l'importo scende nuovamente della metà, raggiungendo 1/4 dell'iniziale.
A 28,5 secondi, dopo un altro tempo di dimezzamento, l'importo diminuisce nuovamente della metà, raggiungendo 1/8 dell'importo iniziale. Infine, dopo 38 secondi, l'importo si dimezza nuovamente, raggiungendo 1/16 dell'importo iniziale, come richiesto nel rendiconto. Pertanto, il tempo necessario è di 38 secondi.
Domanda 2
Nel 2003 è iniziata la ricerca dell'elemento 113 presso il Riken Institute in Giappone. A quel tempo, gli scienziati sono stati in grado di produrre il 278Nh attraverso la fusione di atomi di zinco e bismuto.
Quanti neutroni ci sono nell'isotopo citato?
A) 113
B) 278
C) 391
D) 170
E) 165
Risoluzione:
Alternativa E
Il numero di neutroni può essere calcolato come:
A = Z + n
dove A è il numero di pasta atomico, Z è il numero atomico e n è il numero di neutroni. Sostituendo i valori si ha:
278 = 113 + n
n = 278 - 113
n = 165
Di Stefano Araújo Novais
Insegnante di chimica

