IL oganesson, simbolo Og, numero atomico 118, è l'elemento chimico con il numero atomico più alto nella tavola periodica finora. Non si trova in natura, e la sua produzione è artificiale, quindi è considerato un elemento sintetico. Tuttavia, la sua produzione è molto difficile, ed è considerato un elemento molto raro, essendo stato sintetizzato pochissime volte.
Pur essendo nello stesso gruppo del gas nobili, oganessone non ha molte caratteristiche che si riferiscono a questi elementi, secondo i calcoli i matematici dimostrano, come conseguenza degli effetti relativistici, che subiscono gli elementi superpesanti.
L'elemento 118 è stato sintetizzato per la prima volta nel 2002, attraverso la reazione degli ioni 48Ca con atomi di 249Vedere Il suo nome è un omaggio allo scienziato russo Yuri Oganessian, uno dei più rispettati e riconosciuti nel campo degli elementi superpesanti.
Vedi anche: Rutherfordium — l'elemento chimico sintetico che prende il nome dallo scienziato Ernest Rutherford
Riassunto su oganesson
L'oganessone è un elemento chimico sintetico situato nel gruppo 18 del Tavola periodica.
È stato sintetizzato per la prima volta nel 2002, in un lavoro congiunto tra scienziati russi e americani.
Costituisce il gruppo di elementi più recentemente inseriti nella Tavola Periodica, nel 2016.
È un elemento molto raro, essendo stato sintetizzato pochissime volte.
I loro studi sono ancora molto recenti, con le proprietà di base ancora determinate da calcoli e modelli matematici.
Prove teoriche preliminari indicano che, pur appartenendo al gruppo dei gas nobili, alcune proprietà allontanano Og dagli altri elementi.
La produzione di oganessone avviene da Fusione nucleare, usando ioni di 48Ca e atomi di 249Vedere
Il suo nome è un omaggio allo scienziato russo Yuri Oganessian, uno dei più importanti nel campo dello studio degli elementi superpesanti.
proprietà di oganesson
Simbolo: oh
Numero atomico: 118.
Massa atomica: 294 c.u. (non ufficiale da Iupac).
Configurazione elettronica: [Rn] 7s2 5f14 6d10 7p6.
Isotopo più stabile: 294Og (emivita di 0,69 millisecondi, che può essere aumentata di 0,64 millisecondi o ridotta di 0,22 millisecondi).
Serie chimica: gruppo 18, elementi superpesanti, gas nobili.
Caratteristiche dell'oganesson
Oganesson è il elemento del numero atomico più alto (118) finora ufficializzato dall'Unione Internazionale di Chimica Pura e Applicata (IUPAC). Sebbene sia stato prodotto per la prima volta nel 2002, poco si sa di lui. Molto è ancora ipotizzato, poiché questo elemento non si trova in natura. La sua produzione viene svolta nel laboratorio, che lo configura come elemento sintetico.
Inoltre, il tuo metà vita è inferiore a un millisecondo (10-3 secondo) — ricordando che l'emivita è il tempo necessario affinché l'importo si dimezzi. Pertanto, le proprietà che vengono stabilite per questo elemento non sono altro che i risultati di calcoli teorici basati su modelli matematici, perché nella regione della Tavola Periodica in cui si trova trova il effetti relativistici (la discrepanza tra effetti attesi e osservati come risultato della relatività) sono significativi.
Gli effetti relativistici allontanano Og da ciò che ci si aspettava da lui. L'elemento, ad esempio non ha un comportamento simile ai gas nobili. I calcoli mostrano che l'oganessone sarebbe un solido a temperatura ambiente, con un punto di fusione nell'intervallo 325 ± 15 K (circa 52 °C) e punto di ebollizione nell'intervallo 450 ± 10 K (circa 177 °C).
È anche noto che Og può essere più reattivo di altri gas nobili, poiché gli effetti relativistici gli consentono di perdere più facilmente elettroni di sottolivello p. Un altro punto di disaccordo con i gas nobili è che l'oganessone è a semiconduttore, mentre gli altri sono isolanti.
Leggi anche: Idrogeno: l'elemento chimico che ha il numero atomico più basso nella tavola periodica
Ottenere oganesson
Come altri elementi superpesanti, l'oganesson si ottiene attraverso una tecnica chiamata the fusione a caldo, dove gli ioni dell'isotopo 48Il Ca, presente in natura ma molto poco disponibile, reagisce con isotopi molto più pesanti per produrre gli elementi superpesanti.
Og è un elemento così raro e difficile da ottenere In un arco di dieci anni, solo quattro atomi venne prodotto. In sostanza, la produzione di 294Og, l'unico isotopo conosciuto, si verifica per bombardamento di ioni 48Ca ad un nucleo di 249Cfr, con rilascio di 3 neutroni.
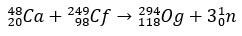
Con pochi millisecondi di emivita, l'Og è stato identificato attraverso il suo modello di decadimento, qualcosa di molto comune per gli elementi super pesanti. In questo caso si sono verificati 3 decadimenti alfa, provocando la trasformazione dell'elemento 118 in copernicio, Cn, che, infine, ha subito la fissione spontanea.
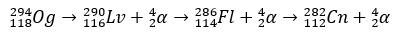
storia di oganesson
La prima sintesi di oganessone è avvenuta nel 2002., nella città di Livermore, California, Stati Uniti, presso il Lawrence Livermore National Laboratory, dove un gruppo di scienziati americani ha collaborato con ricercatori russi del celebre Joint Institute for Nuclear Research (JINR), guidato dallo scienziato russo Yuri Oganessian.
In un periodo di dieci anni dalla prima sintesi, sono stati sintetizzati solo quattro atomi di oganessone, a causa della rarità e difficoltà dei parametri di reazione. Il quarto e ultimo atomo, invece, presentò un'incredibile scoperta.
Gli scienziati stavano cercando di sintetizzare l'elemento 117 attraverso la reazione di 48Ca con il 249Bk, tuttavia è stato notato che il 28% del bersaglio del berkelio ha subito un decadimento β, convertendosi in 249Cf e generando così l'elemento 118. E 'degno di nota il nome dell'elemento 118 onora lo scienziato russo Yuri Oganessian, un tributo che per i chimici viventi si è verificato solo due volte nella storia della chimica, la prima a Glenn Seaborg, con il borgio di mare.
Risolti esercizi su oganesson
domanda 1
L'Oganessone, elemento di numero atomico 118 e simbolo Og, è stato posto nel settimo periodo della Tavola Periodica, nel gruppo dei gas nobili. Di conseguenza, molto è stato speculato sul fatto che un tale elemento presenterebbe una grande stabilità, una caratteristica nota agli altri elementi di questo gruppo. L'assegnazione di Og nel gruppo 18 era dovuta a:
A) questo elemento è altamente stabile.
B) questo elemento ha otto elettroni nel suo guscio di valenza.
C) questo elemento è dimostrabilmente un gas a temperatura ambiente.
D) questo elemento ha le stesse proprietà chimiche degli altri gas nobili.
E) questo elemento ha un'elevata energia di ionizzazione.
Risoluzione:
Alternativa B
L'attribuzione dell'Og avviene solo ed esclusivamente in ragione della sua distribuzione elettronica. Il fatto che contenga otto elettroni strato di valenza, 7 sec2 7p6, lo mette in quella posizione. Gli studi con questo elemento sono ancora preliminari, ma si ipotizza già, a causa di risultati matematici, che Og non sia un gas a temperatura ambiente, per esempio. Un altro punto da sottolineare è che Og non è affatto stabile, nemmeno esistente in natura.
Domanda 2
La grande difficoltà nel produrre l'elemento 118 genera l'idea che gli scienziati fossero in una vera odissea per poterlo rilevare. Non c'è da stupirsi, dopo dieci anni dalla sua prima sintesi, oganesson è stato sintetizzato solo altre tre volte. E finora, è noto un solo isotopo, il 294oh Quanti neutroni ha l'isotopo noto di oganesson?
A) 294.
B) 118.
C) 176.
D) 412.
E) 166.
Risoluzione:
Alternativa C
Il numero di neutroni di Og può essere calcolato come segue:
A = Z + n
A è il numero di pasta atomico, Z è il numero di protoni (o numero atomico) e n è il numero di neutroni. Sostituendo i valori si ha:
294 = 118 + n
n = 294 - 118
n = 176
Di Stefano Araújo Novais
Insegnante di chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/oganessonio-og.htm

