IL tenoso (o tennesso), simbolo Ts, è l'elemento di numero atomico 117 della Tavola Periodica. La sua scoperta è stata molto recente, nel 2009, con il suo inserimento nella Tavola Periodica solo alla fine del 2015. Non si trova in natura sotto forma di nessun isotopo e, quindi, deve essere prodotto in laboratorio, essendo quindi un elemento chimico sintetico.
Le proprietà del Tennesso sono ancora oggetto di studio di chimica teorica e calcoli matematici, data la sua bassa velocità di produzione. La sua produzione avviene attraverso la reazione tra i 48Ca e il 249Bk, essendo possibile produrre l'isotopo 294 o 293 dell'elemento.
Il nome si riferisce allo stato americano del Tennessee, luogo di origine di alcuni scienziati coinvolti nella scoperta e produzione dell'isotopo. 249Bk, così importante per la sintesi di questo nuovo elemento.
Vedi anche: Bohrium — un altro elemento chimico sintetico che ha un basso tasso di produzione
riassunto tennese
Tenesso è un elemento chimico sintetico situato nel gruppo 17 del Tavola periodica.
È stato sintetizzato per la prima volta nel 2009, in un lavoro congiunto tra scienziati russi e americani.
È stato confermato in modo indipendente da scienziati tedeschi.
Costituisce il gruppo di elementi più recentemente inseriti nella Tavola Periodica, nel 2016.
I loro studi sono ancora molto recenti e le loro proprietà vengono stabilite con metodi matematici.
La sua produzione è Fusione nucleare, usando ioni di 48Ca e atomi di 249bk.
Il suo nome si riferisce allo stato americano del Tennessee.
Non fermarti ora... C'è altro dopo l'annuncio ;)
proprietà tennesse
Simbolo: ts.
Numero atomico: 117.
Massa atomica: 293 c.u. o 294 c.u. (non ufficiale Iupac).
Configurazione elettronica: [Rn] 7s2 5f14 6d10 7p5.
Isotopo più stabile:294Ts (51 millisecondi di metà vita, che può variare di 38 millisecondi in più o 16 millisecondi in meno).
Serie chimica: gruppo 17, alogeni, elementi superpesanti.
Caratteristiche Tenesso
Il tennesso (o tennesso), simbolo Ts, era uno degli ultimi quattro elementi da ufficializzare dall'Unione internazionale di chimica pura e applicata (IUPAC) nella sua tavola periodica. Con numero atomico 117, si trova nel gruppo 17 del alogeni.
È stato prodotto per la prima volta tra gli anni 2009 e 2010, ma la sua conferma da parte di Iupac è avvenuta solo il 30 dicembre 2015. Elementi di questa dimensione di numero atomico e numero di neutroni non si trovano in natura, e devono essere creati in laboratorio, quindi è a elemento chimico sintetico.
Il motivo principale per cui non si trovano in natura è che sono estremamente instabili. Una volta prodotti attraverso reazioni nucleari, subiscono decadimento radioattivo in pochi secondi (a volte inferiore a quello, nell'intervallo di millisecondi).
Inoltre, elementi come T vengono prodotti lentamente, con basso rendimento. Nello specifico nel caso del tenesso, i ricercatori hanno mantenuto la reazione per 70 giorni in modo da rilevare sei atomi di questo elemento.
Pertanto, in questo momento, i ricercatori stanno cercando di determinare le proprietà di base di Ts e alcuni dei suoi composti attraverso calcoli teorici e modelli matematici. In uno studio condotto e pubblicato in Lettere di Fisica Chimica, il ricercatore brasiliano Robson Fernandes de Farias ha stimato alcune proprietà fisiche di Ts e tennesso, TsH, come raggio covalente, polarizzabilità, distanza del legame covalente e energia del legame covalente.
Saperne di più: Oganessone: l'elemento chimico con il numero atomico più alto nella tavola periodica
ottenendo teneso
Gli elementi superpesanti come il teneso sono ottenuti con una tecnica chiamata reazione di fusione calda (traduzione libera di reazione di fusione calda). In questa tecnica, è comune utilizzare gli ioni 48Ca, un isotopo stabile di calcio, con un'abbondanza naturale dello 0,2% e otto neutroni in più rispetto all'isotopo convenzionale.
Per Ts, gli ioni 48Ca ha reagito con l'isotopo 249Bk, un attinide. Così, inizialmente, il 297Ts, che decadde rapidamente e perse tre o quattro neutroni, formando gli isotopi 294T e 293ts.
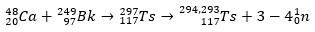
È stato possibile verificare tutto questo con il analisi delle catene di decadimento α, che ha raggiunto il dubnio e Roentgen. Poiché gli isotopi Ts ottenuti sono instabili, subiscono spontaneamente reazioni di decadimento α, o cioè emettono una particella α (che ha due protoni e due neutroni) fino a raggiungere nuclei stabili.
Con la scia di decadimento, gli scienziati sono stati in grado di mettere insieme il puzzle e quindi confermare l'esistenza dell'elemento superpesante. per l'isotopo 293Ts, c'erano tre decadimenti α fino al 281Rg, mentre per l'isotopo 294Ts erano sei decadimenti α al 270DB
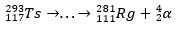
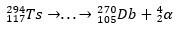
storia di teneso
Elemento 117, la prima volta, è stato realizzato attraverso una vasta cooperazione internazionale tra scienziati russi e americani, che ha avuto luogo presso i locali del Laboratorio Flerov per le reazioni nucleari (FLNR), situato presso l'Istituto congiunto per la ricerca nucleare, nella città di Dubna, in Russia.
E 'degno di nota indipendentemente, i risultati sono stati ulteriormente confermati da scienziati tedeschi dal Centro Helmhotz per la ricerca sugli ioni pesanti (GSI), con sede a Darmstadt, in Germania. Per 70 giorni, nel 2009, il team di scienziati dell'FLNR ha reagito con ioni di 48Ca con atomi di 249Bk per ottenere così sei atomi dell'elemento 117. Quindi, nel 2012, gli scienziati sono riusciti a ottenere sette atomi dell'elemento 117.
La conferma indipendente del GSI è dovuta ad un altro tentativo: gli scienziati stavano cercando di produrre l'elemento 119, che aprirebbe l'ottavo periodo della Tavola Periodica. In questo caso, l'idea era di reagire con uno ione di 50Te con un obiettivo di 249bk. Tuttavia, nonostante gli sforzi, questo elemento non è stato rilevato dopo quattro mesi di tentativi.
Cambiare gli ioni di titanio di 48Ca, gli scienziati del GSI sono andati alla ricerca di un elemento superpesante raro ma noto per verificare le loro procedure sperimentali. Così, hanno finito per sintetizzare l'elemento 117, che è servito a questo elemento per essere confermato da Iupac.
IL Il nome tenesso è un riferimento allo stato americano del Tennessee.Questo è stato un modo non solo per onorare l'origine di alcuni scienziati coinvolti negli esperimenti FLNR, ma anche per ricordare il luogo in cui gli isotopi di 249Bk, così cruciali per la scoperta, sono stati sintetizzati mentre venivano prodotti presso l'Oak Ridge National Laboratory. In inglese, il nome dell'elemento è tennessina, il cui suffisso accompagna gli altri alogeni: fluoro, cloro, bromo, iodio, e astato.
Esercizi risolti su teneso
domanda 1
Tenesso, simbolo Ts, è l'elemento più recentemente incluso nel gruppo degli alogeni (gruppo 17). Pertanto, ci si aspetta che, in base alle proprietà periodiche, abbia un comportamento chimico simile a quello degli elementi di questo gruppo. Pertanto, tra le seguenti alternative, si può affermare che teneso:
A) ha sei elettroni di valenza.
B) ha il raggio atomico più piccolo tra gli elementi di questo gruppo.
C) ha l'elettronegatività più bassa tra gli elementi di questo gruppo.
D) ha bisogno di tre elettroni per raggiungere l'intero ottetto.
E) ha la più alta affinità elettronica del gruppo 17.
Risoluzione:
Alternativa C
Ts ha, come tutti gli elementi del gruppo 17, sette elettroni nel strato di valenza, avendo come strato di valenza lo strato 7s2 7p5. Pertanto, si può concludere che avrebbe bisogno di un elettrone per raggiungere l'ottetto, poiché ha sette elettroni nel suo guscio di valenza.
Essendo l'elemento con il maggior numero di gusci di elettroni tra gli alogeni, Ts ha anche il più alto raggio atomico, che garantisce meno affinità elettronica, poiché gli elettroni aggiunti sarebbero abbastanza lontani dal nucleo. Il raggio più piccolo fa sì che tennesso abbia anche l'elettronegatività più bassa di tutti gli elementi del gruppo 17.
Domanda 2
Teneso, simbolo Ts e numero atomico 117, è stato rilevato per la prima volta dalla formazione di due dei suoi isotopi: massa 293 e massa 294. Pertanto, è possibile dire che il numero di neutroni nel 293Ts e da 294Ts è rispettivamente uguale a:
A) 293 e 294
B) 117 e 118
C) 177 e 294
D) 176 e 177
E) 176 e 293
Risoluzione:
Alternativa D
Il numero di neutroni dei due isotopi può essere determinato come:
A = Z + n
A è il numero di pasta atomico, Z il numero di protoni (numero atomico) e n è il numero di neutroni.
Sostituendo l'isotopo 293, abbiamo:
293 = 117 + n
n = 293 - 117
n = 176
Per l'isotopo 294 abbiamo:
294 = 117 + n
n = 294 - 117
n = 177
Di Stefano Araújo Novais
Insegnante di chimica

