Le trasformazioni gassose sono processi in cui a gas può avere uno o più dei suoi parametri da pressione, volume e temperaturacambiato. Esistono particolari trasformazioni gassose in cui almeno una di queste quantità è mantenuta costante.
I tipi di trasformazioni del gas sono:
trasformazione isobarica;
trasformazione isotermica;
trasformazione isovolumetrica;
trasformazione adiabatica.
Vedi anche:Termologia — lo studio dei fenomeni legati al calore e alla temperatura
trasformazione isotermica
La trasformazione isotermica è quella in cui il la temperatura di un gas rimane costante. In questo tipo di trasformazione, pressione e volume sonoinversamenteproporzionale, in modo che aumentando il pressione, il volume viene ridotto e viceversa.
Le trasformazioni isoterme sono descritte da lhey boyle-mariotte. Secondo questa legge, il prodotto tra pressione e volume di un gas ideale è costante:

PERio e PERF – pressione iniziale e finale
Vio e VF – velocità iniziale e finale
K - costante
trasformazione isobarica
La trasformazione isobarica è caratterizzata da a variazione di volume e temperatura, mantenendo la pressione costante. Questo tipo di trasformazione è matematicamente descritto dalla legge di Charles e Gay-Lussac. Durante una trasformazione isobarica, temperatura e volume sono direttamente proporzionali, cioè mantenendo costante la pressione di un gas, il volume da esso occupato aumenterà con l'aumentare della temperatura del gas. gas.
Guarda la formula usata da Legge Gay-Lussac:
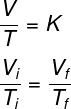
Tio e TF – temperatura iniziale e finale
Secondo il Legge di Gay-Lussac, il rapporto tra il volume e la pressione di un gas, durante una trasformazione isobarica, è uguale a una costante.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Trasformazione isovolumetrica
Trasformazione isovolumetrica, isometrica o isocora è il nome del processo in cui un gas ideale subisce variazioni di pressione e temperatura, mantenendosi costante tuo volume. Questo tipo di trasformazione del gas, che avviene all'interno di contenitori a pareti rigide, è matematicamente definita dalla legge di Carlo.
Secondo questa legge, il rapporto tra pressione e temperatura di un gas ideale è sempre costante. Inoltre, in questo tipo di trasformazione, la pressione e la temperatura sono direttamente proporzionale: raddoppiando la pressione, raddoppiamo la temperatura e viceversa.
La formula che descrive il comportamento dei gas ideali durante le trasformazioni isovolumetriche è la seguente:
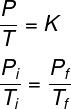
Leggi anche: Termodinamica — un'area della fisica che studia i fenomeni in cui c'è scambio di calore
trasformazione adiabatica
Trasformazione adiabatica è il nome del processo subito da a gas che non cambia calore con l'ambiente esterno o con le pareti del suo contenitore. La formula che spiega matematicamente il comportamento di un gas ideale che subisce una trasformazione adiabatica afferma che il prodotto tra pressione e volume elevato a costante γ è costante.

La costante dipende da gradiinlibertà del gas, cioè il numero di direzioni in cui le molecole di gas possono muoversi. Può anche essere calcolato dal rapporto tra il calore specifico in pressionecostante e calorespecifica in volumecostante.
Esempi di trasformazioni di gas
trasformazione isotermica – qualsiasi lenta espansione o contrazione di un gas che si verifica a temperatura costante.
trasformazione isobarica – raffreddare il gas contenuto in una sacca posta a raffreddare in frigorifero.
Trasformazione isovolumetrica – riscaldare completamente il vapore acqueo confinato in una pentola a pressione.
trasformazione adiabatica – gas espulso da uno spray aerosol.

Vedi anche: Calorimetria – formule, concetti ed esercizi risolti
Esercizi risolti sulle trasformazioni dei gas
Domanda 1 - Esamina le alternative di seguito e controlla la risposta che contiene solo alternative vere.
I – Le trasformazioni isotermiche sono quelle in cui la temperatura del gas è mantenuta costante.
II – Le trasformazioni adiabatiche comportano lo scambio termico tra il gas e l'ambiente esterno.
III – La trasformazione isocora è quella in cui la pressione del gas è mantenuta costante.
IV – Le trasformazioni isobariche avvengono con pressione costante.
Sono corretti:
a) I e II.
b) I, II e III.
c) II e III.
d) I e IV.
Risoluzione:
Le alternative II e III sono sbagliate, poiché le trasformazioni adiabatiche non comportano scambio termico e le trasformazioni isocore sono quelle che avvengono a volumi costanti. Quindi, l'alternativa corretta è il lettera D
Domanda 2 -Un gas ideale subisce una rapida trasformazione, cosicché la sua temperatura, pressione e volume subiscono brusche variazioni in un breve periodo di tempo. Secondo la sua conoscenza delle trasformazioni del gas, la trasformazione subita dal gas era:
a) isoterma.
b) isobarico.
c) adiabatico.
d) isovolumetrico.
Risoluzione:
Le trasformazioni adiabatiche avvengono rapidamente, quindi non c'è tempo per il gas di scambiare calore con l'ambiente esterno. In questo tipo di trasformazione i parametri di pressione, volume e temperatura cambiano bruscamente. Quindi, l'alternativa corretta è il lettera C
Di Rafael Hellerbrock
Insegnante di fisica
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Aspetto:
HELERBROCK, Rafael. "Trasformazioni di gas"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/quimica/transformacoes-gasosas.htm. Consultato il 27 luglio 2021.



