Le piogge acide sono un fenomeno causato dall'inquinamento atmosferico. Principalmente attraverso la combustione di combustibili fossili nelle industrie e nelle automobili, gli esseri umani hanno rilasciato una grande quantità di gas inquinanti, come alcuni ossidi.
Gli ossidi sono composti inorganici binari che hanno l'ossigeno come elemento più elettronegativo. Tra questi abbiamo una classe che sono gli ossidi acidi, che vengono chiamati così perché reagiscono con l'acqua, generando acidi, e reagiscono anche con le basi, formando acqua e sale.
I principali ossidi acidi rilasciati in atmosfera e che reagiscono con l'acqua piovana, producendo piogge acide, sono i ossidi di zolfo (SO2 e così3) e azoto (N2O, NO e NO2).
Mappa mentale: pioggia acida

*Per scaricare la mappa mentale in PDF, Clicca qui!
I più grandi cattivi sono gli ossidi di zolfo, perché, come mostrano le equazioni chimiche sottostanti, reagiscono con acqua e formano acido solforico, lo stesso acido utilizzato nelle batterie delle auto, che è molto acido. forte:
S(S) + O2(g) → Sistema operativo2(g)
SOLTANTO2(g) + H2oh(1)→ HSO3(ac) (acido solforico)
SOLTANTO2(g)+ ½ il2(g) → Sistema operativo3(g)
SOLTANTO3(g) + H2oh(1)→ h2SOLTANTO4(ac)(Acido solforico)
Gli ossidi di azoto reagiscono con l'acqua piovana per formare acido nitrico (HNO3) e acido nitroso (HNO2), che, nel tempo, può causare un certo impatto ambientale.
n2(g) + 2 O2(g) → 2 NO2(g)
AL2(g) + H2oh(1)→ HNO2(ac) + HNO3(ac)
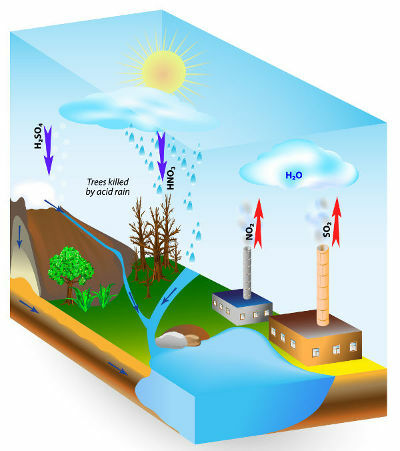
Schema delle cause della pioggia acida
Questo termine "pioggia acida" fu usato per la prima volta dal chimico e climatologo inglese Robert Angus Smith nel descrivere la precipitazione acida avvenuta su Manchester all'inizio della rivoluzione industriale.
Infatti, tutte le piogge sono acide, in quanto il pH della sua acqua è naturalmente inferiore a 7, soprattutto intorno a 5,6, data la normale presenza di anidride carbonica (CO2) nell'atmosfera, che reagisce con l'acqua e genera acido carbonico (H2CO3), un acido debole.
Ciò nonostante, tecnicamente si chiama “pioggia acida” qualsiasi pioggia che acquisisca un pH inferiore a 4,5.
La preoccupazione relativa al verificarsi di piogge acide si verifica perché provoca diversi danni ambientali, portando problemi per le piante, distruggendo foglie e rami di alberi, per il suolo, provocandone l'alterazione chimica, per le acque dei fiumi e laghi, portando alla morte dei pesci, contaminando anche le acque sotterranee, oltre ad essere correlato all'insorgere di malattie respiratorio.
Oltre a questo danno ambientale, le piogge acide reagiscono con i carbonati, come il marmo (calcare – carbonato di calcio – CaCO3) che compongono le statue, i monumenti storici e molti materiali utilizzati nell'edilizia civile, che nel tempo si sono degradati. Reagiscono anche con i metalli, distruggendo le strutture metalliche di edifici e ponti.

Muro di calcare corroso dal tempo e dalle piogge acide
di Jennifer Fogaça
Laureato in Chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-chuva-acida.htm
