IL Tavola periodica è un modello che raggruppa tutti gli elementi chimici conosciuti e le loro proprietà. Sono disposti in ordine crescente di numeri atomici (numero di protoni).
In totale, la nuova tavola periodica ha 118 elementi chimici (92 naturali e 26 artificiali).
Ogni quadrato specifica il nome dell'elemento chimico, il suo simbolo e il suo numero atomico.
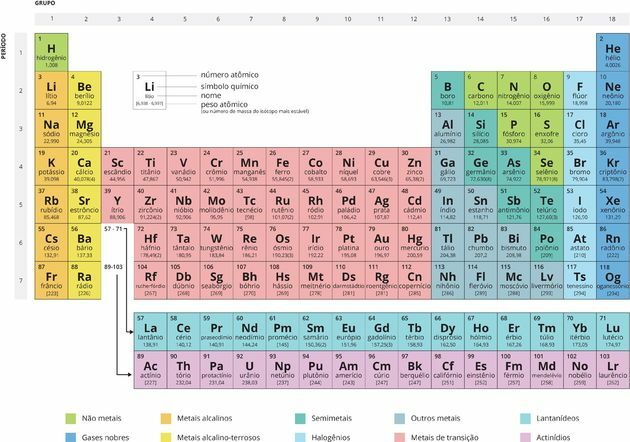
Organizzazione della tavola periodica
le chiamate periodi sono linee orizzontali numerate, che hanno elementi che hanno lo stesso numero di strati elettronici, per un totale di sette periodi.
- 1° periodo: 2 elementi
- 2° periodo: 8 elementi
- 3° periodo: 8 elementi
- 4° Periodo: 18 elementi
- 5° Periodo: 18 elementi
- 6° periodo: 32 elementi
- 7° periodo: 32 elementi
Con l'organizzazione dei periodi nella tabella, alcune linee orizzontali diventerebbero molto lunghe, quindi è comune rappresentare la serie dei lantanidi e la serie degli attinidi separatamente dalle altre.
A Famiglie o gruppi sono le colonne verticali, dove gli elementi hanno lo stesso numero di elettroni nel guscio più esterno, cioè nel
strato di valenza. Molti elementi di questi gruppi sono correlati secondo la loro proprietà chimiche.Ci sono diciotto Gruppi (A e B), e le famiglie più note sono del Gruppo A, chiamato anche elementi rappresentativi:
- 1A Famiglia: Metalli Alcalini (litio, sodio, potassio, rubidio, cesio e francio).
- 2A Famiglia: Metalli alcalino-terrosi (berillo, magnesio, calcio, stronzio, bario e radio).
- Famiglia 3A: Famiglia Boro (boro, alluminio, gallio, indio, tallio e nihonium).
- Famiglia 4A: Famiglia del carbonio (carbonio, silicio, germanio, stagno, piombo e flerovio).
- Famiglia 5A: Famiglia dell'azoto (azoto, fosforo, arsenico, antimonio, bismuto e muscovio).
- Famiglia 6A: Calcogeni (ossigeno, zolfo, selenio, tellurio, polonio, livermorio).
- Famiglia 7A: Alogeni (fluoro, cloro, bromo, iodio, astato e tenesina).
- Famiglia 8A: Gas nobili (Elio, Neon, Argon, Krypton, Xenon, Radon e Oganessonium).
voi elementi di transizione, detti anche metalli di transizione, rappresentano le 8 famiglie del Gruppo B:
- famiglia 1B: rame, argento, oro e roentgen.
- famiglia 2B: zinco, cadmio, mercurio e copernico.
- Famiglia 3B: scandio, ittrio e serie di lantanidi (15 elementi) e attinidi (15 elementi).
- Famiglia 4B: titanio, zirconio, afnio e rutherfordio.
- famiglia 5B: vanadio, niobio, tantalio e dubnio.
- Famiglia 6B: cromo, molibdeno, tungsteno e seaborgio.
- Famiglia 7B: manganese, tecnezio, renio e bohrio.
- famiglia 8B: ferro, rutenio, osmio, hassio, cobalto, rodio, iridio, meitnerio, nichel, palladio, platino, darmstadium.
Per decisione dell'Unione Internazionale di Chimica Pura e Applicata (IUPAC), i gruppi hanno iniziato ad essere organizzati per numeri da 1 a 18, anche se è ancora comune trovare famiglie descritte da lettere e numeri come mostrato sopra.
Un'importante differenza generata dal nuovo sistema presentato da IUPAC è che la famiglia 8B corrisponde ai gruppi 8, 9 e 10 nella tavola periodica.
Tavola periodica in bianco e nero
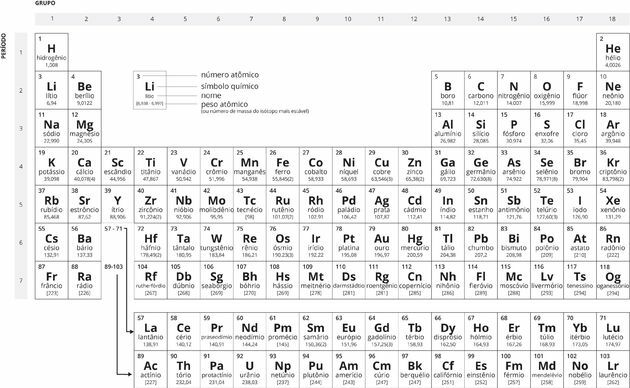
Storia della tavola periodica
Lo scopo fondamentale della creazione di una tabella era quello di facilitare la classificazione, l'organizzazione e il raggruppamento degli elementi in base alle loro proprietà.
Fino a raggiungere il modello attuale, molti scienziati hanno creato tabelle che potrebbero dimostrare un modo per organizzare gli elementi chimici.
La tavola periodica più completa è stata redatta dal chimico russo Dmitri Mendeleev (1834-1907), nell'anno 1869 a causa del massa atomica degli elementi.
Mendeleev organizzò gruppi di elementi secondo proprietà simili e lasciò spazi vuoti per elementi che riteneva sarebbero stati scoperti.
La tavola periodica come la conosciamo oggi è stata organizzata da Henry Moseley, nel 1913, per ordine di numero atomico elementi chimici, riorganizzando la tavola proposta da Mendeleev.
William Ramsay scoprì gli elementi neon, argon, krypton e xeno. Questi elementi insieme all'elio e al radon includevano la famiglia dei gas nobili nella tavola periodica.
Glenn Seaborg scoprì gli elementi transuranici (numeri dal 94 al 102) e nel 1944 propose la riconfigurazione della Tavola Periodica, ponendo la serie degli attinidi al di sotto della serie dei lantanidi.
Nel 2019, la tavola periodica compie 150 anni ed è stata creata una risoluzione delle Nazioni Unite e dell'UNESCO per rendere questo l'Anno Tavola periodica internazionale degli elementi chimici come modo per riconoscere una delle creazioni più influenti e importanti di Scienze.
Curiosità della tavola periodica
- L'Unione Internazionale di Chimica Pura e Applicata Unione Internazionale di chimica pura e applicata - IUPAC) è una ONG (Organizzazione non governativa) dedicata a studi e progressi in Chimica. A livello mondiale, lo standard stabilito per la tavola periodica è raccomandato dall'Organizzazione.
- 350 anni fa, il primo elemento chimico isolato in laboratorio fu il fosforo dall'alchimista tedesco Henning Brand.
- L'elemento plutonio è stato scoperto negli anni '40 dal chimico americano Glenn Seaborg. Scoprì tutti gli elementi transuranici e vinse il Premio Nobel nel 1951. L'elemento 106 è stato chiamato Seaborgio in suo onore.
- Nel 2016 sono stati ufficializzati nuovi elementi chimici della tavola: Tennessine (Ununséptio), Nihonium (Ununtrio), Moscovium (Ununpêntio) e Oganesson (Ununóctio).
- I nuovi elementi chimici sintetizzati sono detti super pesanti perché contengono un alto numero di protoni, che risulta essere di gran lunga superiore agli elementi chimici presenti in natura.
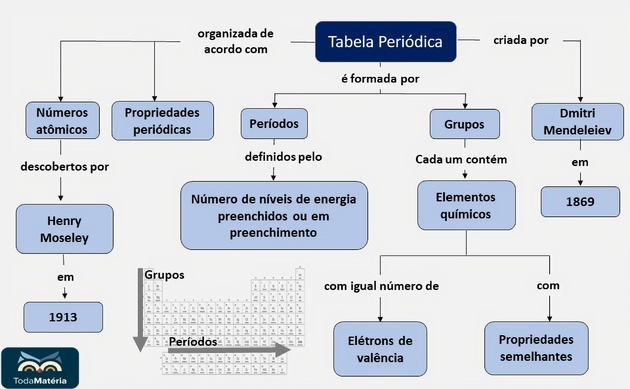
Riepilogo della tavola periodica
Controlla le domande dell'esame di ammissione con una risoluzione commentata in Esercizi sulla tavola periodica e domande inedite in Esercizi sull'organizzazione della tavola periodica.

