ammine sono composti organici azotati che derivano dalla sostanza ammoniaca (NH3) sostituendo uno o più idrogeni con radicali organici. Secondo la quantità di idrogeni sostituiti, il ammine possono essere classificati in:
Ammina primaria: formato sostituendo un idrogeno in ammoniaca con un radicale organico;
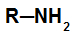
Struttura generale di un'ammina primaria
Ammina secondaria: formato dalla sostituzione di due idrogeni ammoniacali con due radicali organici.

Struttura generale di un'ammina secondaria
Ammina terziaria: formato sostituendo i tre idrogeni dell'ammoniaca con tre radicali organici.

Struttura generale di un'ammina terziaria
Caratteristiche fisiche delle ammine
Sono composti polari;
Le ammine primarie e secondarie sono in grado di svolgere legami di idrogeno;
Le ammine terziarie effettuano l'interazione dipolo permanente;
Le ammine con un massimo di cinque atomi di carbonio sono solubili in acqua ed etanolo. Le ammine con sei o più atomi di carbonio sono praticamente insolubili in acqua, ma solubili in solventi organici;
Le ammine che hanno una struttura aromatica sono più dense dell'acqua;
Le ammine con uno o tre atomi di carbonio sono gassose a temperatura ambiente. Quelli da quattro a dodici atomi di carbonio sono liquidi a temperatura ambiente;
In generale, le ammine hanno punti di fusione e di ebollizione più elevati solo in relazione a qualsiasi composto organico non polare.
Caratteristiche chimiche delle ammine
Sono considerate basi organiche, secondo la teoria di Bronsted-Lowry;
Le ammine aromatiche hanno un carattere basico inferiore a causa del fenomeno di risonanza;
Maggiore è il carattere basico dell'ammina, più è probabile che reagisca con una certa sostanza;
In presenza di un acido, le ammine svolgono reazione di neutralizzazione, poiché hanno un carattere di base.
regola di nomenclatura delle ammine
Per nominare un'ammina, seguire semplicemente la regola stabilita dall'Unione internazionale di chimica pura e applicata (IUPAC), descritta di seguito:
Nome del radicale o dei radicali + ammina
NOTA: Se l'ammina ha radicali diversi, dobbiamo seguire l'ordine alfabetico.
Segui alcuni esempi:
Esempio 1: ammina primaria

Nell'ammina primaria in questo esempio, abbiamo la presenza di un radicale propilico, quindi il suo nome è propilammina.
Esempio 2: ammina secondaria

Nell'ammina secondaria in questo esempio abbiamo la presenza del radicale metile (a sinistra dell'azoto) e del radicale etilico (a destra dell'azoto). Il suo nome è, in ordine alfabetico, etil-metilammina.
Esempio 3: ammina terziaria
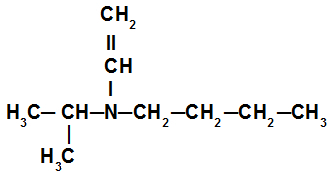
Nell'ammina secondaria in questo esempio, abbiamo il radicale isopropilico (a sinistra dell'azoto), il radicale butilico (a destra dell'azoto) e il radicale vinilico (sotto l'azoto). Il suo nome è quindi butil-isopropil-vinilammina.
Applicazioni di ammina
Ampiamente usato nella produzione di vari composti organici;
Utilizzato nella fabbricazione di saponi;
Utilizzato nel processo di vulcanizzazione della gomma;
Utilizzato nella produzione di coloranti.
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-aminas.htm
