La Terza Legge della Termodinamica si occupa del comportamento della materia con un'entropia prossima allo zero.
Secondo questa legge, ogni volta che un sistema è in equilibrio termodinamico, la sua entropia tende a zero.
La seconda legge della termodinamica riguarda l'entropia. Successivamente, la terza legge appare come a tentare di stabilire un punto di riferimento assoluto che determini l'entropia.
Walther Nernst (1864-1941) fu il fisico che si occupò dei principi che costituirono la base della terza legge della termodinamica.
Secondo Nernst, l'entropia tenderebbe ad avere un valore minimo se la temperatura di una sostanza pura fosse uguale o prossima allo zero assoluto.
Per questo, Nernst ha proposto la formula seguente, che mostra che la variazione di entropia (ΔS) e temperatura (T) tendono a valori minimi, cioè 0:
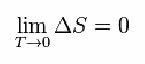
Ma cos'è l'entropia?
entropia è il modo in cui le molecole si organizzano nel sistema. Questa organizzazione si traduce in disordine, non nel senso di confusione, ma nel senso di movimento e agitazione delle molecole.
Più molecole possono muoversi, più sono disorganizzate, più entropia hanno.
Inizialmente, Nernst suggerì che l'entropia da lui proposta sarebbe stata possibile solo su cristalli perfetti.
Infine, ha concluso che la temperatura pari allo zero assoluto non esisteva, il che rende la terza legge una legge controversa.
Quindi, per molti fisici, questa non è una legge ma una regola.
Dopo tanti anni (dal 1912), gli scienziati stanno cercando di ottenere questa temperatura o temperature che si avvicinano sempre di più allo zero assoluto. Così, hanno scoperto che è possibile solo nei gas, scartando qualsiasi sostanza allo stato solido o liquido.
Leggi anche:
- Legge zero della termodinamica
- Prima Legge della Termodinamica
- Seconda Legge della Termodinamica
- Esercizi di Termodinamica