L'ossidazione è la reazione chimica in cui atomi, ioni o molecole perdono elettroni. Inoltre provoca un aumento del numero di ossidazioni (nox).
Il termine ossidazione è stato inizialmente creato per indicare reazioni in cui l'ossigeno era il reagente. Tuttavia, è stato riscontrato che in alcuni casi si sono verificati in assenza di questo elemento. Poiché il termine era già ampiamente noto, continuò ad essere utilizzato.
Le reazioni di ossidazione si verificano contemporaneamente alle reazioni di riduzione. Pertanto, sono chiamati redox, in cui vengono trasferiti gli elettroni.
Nelle reazioni redox, l'agente ossidante è quello che accetta gli elettroni, subendo una riduzione. L'agente riducente perde elettroni e subisce ossidazione.
Esempi di ossidazione
ossidazione del ferro
La ruggine è l'ossidazione del ferro. Tutti i metalli possono subire ossidazione. Si verifica a causa del contatto dei metalli con aria e acqua. Inizialmente, il corrosione che è l'usura del metallo dovuta all'ossidazione. Quindi, forma il ruggine.
Guarda la reazione di redox per formazione di ruggine:
- Fe(s) → Fe2+ + 2e-. In questa fase il ferro perde due elettroni, subisce ossidazione
- oh2 + 2 H2O + 4e- → 4OH-. O riduzione2
- 2Fe + O2 + 2H2O → 2 Fe(OH)2. Equazione generale - Fe(OH)2 è l'Idrossido di Ferro, responsabile del colore bruno della ruggine.
Per proteggere il ferro e l'acciaio dall'ossidazione si può utilizzare la tecnica della zincatura. È costituito da un rivestimento di zinco metallico. Tuttavia, è un processo costoso, che in alcuni casi lo rende irrealizzabile.
Pertanto, gli scafi delle navi e delle piattaforme metalliche ricevono blocchi metallici di magnesio che impediscono l'ossidazione del ferro. Il magnesio è considerato un metallo sacrificale e deve essere sostituito di tanto in tanto quando si consuma.
La verniciatura può anche proteggere il metallo dall'ossidazione, ma non è altrettanto efficace.

Ruggine
Leggi anche su Acciaio inossidabile e Leghe metalliche.
Ossidazione in chimica organica
Oltre ai metalli, l'ossidazione può verificarsi anche con Idrocarburi, in particolare il alcheni. L'ossidazione organica ha quattro forme: combustione, ozonolisi, ossidazione lieve e ossidazione energetica.
Combustione
IL combustione è una reazione chimica di una sostanza con l'ossigeno, che culmina nella produzione di luce e calore. L'ossigeno è chiamato ossidante. La sostanza con il carbonio è il carburante.
L'ossigeno ha la funzione di ossidare il combustibile, è l'agente ossidante della combustione.
La combustione può essere completa o incompleta. Conoscere la differenza tra i due modi:
- Combustione completa: Si verifica quando l'apporto di ossigeno è sufficiente. Al termine della reazione, l'anidride carbonica (CO2) e acqua (H2O).
- Combustione incompleta: Non c'è abbastanza ossigeno, si formano monossido di carbonio (CO) e acqua (H2O).
Ozonolisi
In questo tipo di reazione, l'ozono è il reagente che provoca l'ossidazione degli alcheni. Si verifica la rottura del doppio legame degli alcheni e la formazione di composti carbonilici, come aldeidi e chetoni.
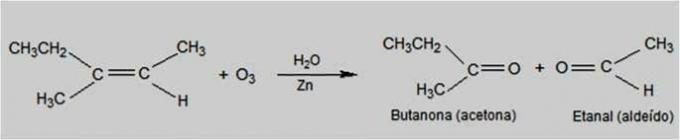
Reazione di ozonolisi
lieve ossidazione
L'ossidazione lieve si verifica quando l'agente ossidante è un composto come il permanganato di potassio (KMnO4), presente in soluzione acquosa, diluita e raffreddata, neutra o leggermente basica.
Questo tipo di ossidazione avviene utilizzando il Baeyer Test, utilizzato per differenziare gli alcheni dai ciclani isomerici.
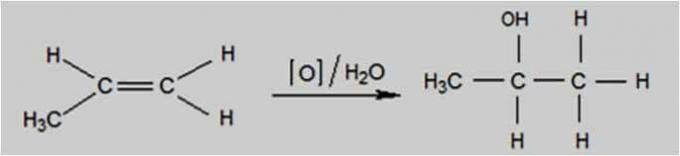
Reazione di ossidazione lieve
Ossidazione energetica
In questo tipo di ossidazione il permanganato di potassio si trova in un ambiente più caldo e più acido, rendendo la reazione più energica. Gli agenti ossidanti energetici possono rompere il doppio legame degli alcheni.
A seconda della struttura dell'alchene, si possono formare chetoni e acidi carbossilici.
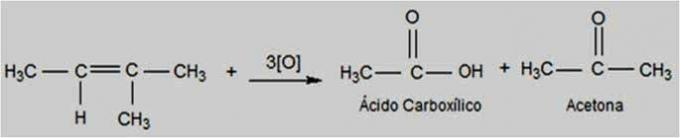
Reazione di ossidazione energetica
Voglio sapere di più? Leggi anche su Elettrochimica.



