Il carbonio è un elemento chimico con numero atomico (Z) pari a 6, il che significa che gli atomi che lo compongono hanno sei protoni nel loro nucleo. La sua massa molare è di 12.011 g/mol e in natura si trovano tre isotopi del carbonio, che sono: o carbonio-12, carbonio-13 e carbonio-14. C-12 ha sei protoni e sei neutroni nel nucleo ed è il più abbondante.
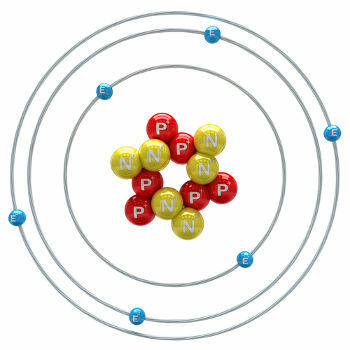
atomo di carbonio-12 illustrazione
C-13 ha sette neutroni ed è il meno abbondante (da 1,01 a 1,14%). Il C-14 ha otto neutroni ed è a elemento radioattivo che emette particelle (elettroni), formandosi nella stratosfera terrestre quando i neutroni dei raggi cosmici bombardano l'Azoto-14 presente in questi strati superiori dell'atmosfera. È incorporato da tutte le piante e gli animali e, sapendo che la sua emivita è di circa 5730 anni, viene utilizzato per determinare l'età dei fossili tra 100 e 40.000 anni. Maggiori dettagli su C-14 e la tecnica di datazione possono essere visti nel testo. Cos'è il carbonio-14?
Il carbonio è tetravalente, cioè ha bisogno di altri quattro protoni nel suo strato di valenza (strato più esterno) per obbedire alla regola dell'ottetto. Pertanto, di solito forma quattro legami covalenti, condividendo quattro coppie di elettroni con altri elementi e altri atomi di carbonio. Questi legami possono essere singoli, doppi o tripli e danno luogo alla formazione di milioni di composti diversi. Per questo motivo è stata creata un'area di Chimica, la
Chimica organica, che studia i principali composti derivati dal carbonio, ad eccezione di alcuni casi di origine minerale, come anidride carbonica (CO2), O monossido di carbonio (CO), O carbonato di calcio (CaCO3), bicarbonato di sodio o bicarbonato di sodio (NaHCO3), tra gli altri. Questi composti sono studiati in Chimica inorganica.Il carbonio esegue l'allotropia, formando sostanze semplici, cioè sostanze che sono formate solo da legami tra atomi di carbonio. Esistono almeno sette allotropi del carbonio, che sono grafite (alfa e beta), diamante, lonsdaleite (diamante esagonale), caoite, carbonio (VI) e fullereni. Esistono in realtà diversi tipi di fullereni, che sono forme allotropiche sintetiche di carbonio. Hanno una struttura poliedrica con un atomo di carbonio ad ogni vertice e un esempio è il Ç60 chiamato buckminsterfullerene, e la sua struttura sembra un pallone da calcio.
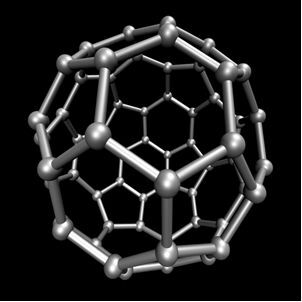
Carbon-60 (buckminsterfullerene)
Tuttavia, tra questi allotropi del carbonio, ce ne sono solo due naturali. grafiteViene da Diamante. Differiscono solo per la disposizione cristallina degli atomi nello spazio, come mostrato nella figura sottostante, e questo si traduce in proprietà fisico-chimiche totalmente diverse. Leggi il prossimo allotropia del carbonio per maggiori informazioni.

Le due forme allotropiche naturali del carbonio sono la grafite e il diamante.
Un'altra forma allotropica sintetica di carbonio è il nanotubi (immagine sotto) che hanno ampie applicazioni biologiche, tra cui diagnostica e trattamenti medici.

Illustrazione di un microscopico nanotubo di carbonio
Così, il carbonio è presente in tutto ciò che ci circonda e dentro di noi, perché compone composti organici naturali — come i combustibili fossili, che includono petrolio, carbone e gas naturale, e altri combustibili come etanolo e biocarburanti — prodotti agricoli, tra gli altri. anche la forma composti organici sintetici, come le fibre sintetiche che compongono i tessuti, i medicinali, i polimeri che compongono le plastiche e le gomme, gli insetticidi, i coloranti e molto altro. Dentro di noi, animali e vegetali, il carbonio forma composti molto importanti, come i carboidrati, come lo zucchero, il glucosio e la cellulosa; le proteine che formano, ad esempio, il DNA, e insieme ai lipidi formano le membrane dei globuli rossi e dei globuli bianchi.
Tutto questo mostra l'importanza del carbonio per sostenere la vita. Ma è stato anche associato ad aspetti negativi, come l'intensificazione del effetto serra e il conseguente il riscaldamento globale, questo perché il principale nemico di questi problemi è il suo composto di anidride carbonica (CO2). Principalmente a causa della grande combustione di combustibili fossili che rilasciano questo gas, la concentrazione di CO2 nell'atmosfera è aumentata. Essendo un gas serra, causa i problemi menzionati. D'altra parte, l'anidride carbonica è presente anche in reazioni vitali come la fotosintesi e la respirazione.
di Jennifer Fogaça
Laureato in Chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-carbono.htm

