Possiamo notare che ogni volta che aumentiamo la concentrazione di uno o di tutti i reagenti che partecipano a una reazione chimica, si ha un aumento della sua velocità di sviluppo, cioè della velocità della reazione.
È vero anche il contrario. Ad esempio, attualmente si consiglia di utilizzare gel alcolico al posto dell'alcol normale, poiché c'è meno rischio che si bruci e quindi si evitino incidenti. L'alcol liquido ordinario è in realtà una miscela di alcol e acqua, con alcol gel contenente una quantità minore di alcol. Pertanto, quando si riduce la concentrazione di uno dei reagenti di combustione, nel caso dell'alcol, la reazione procede più lentamente. D'altra parte, più puro è l'alcol, più rapida è la reazione di combustione.

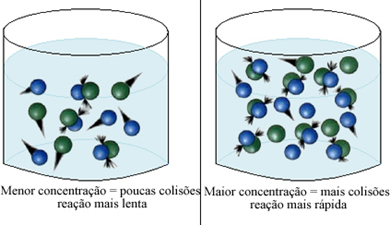
Come indicato nel testo Condizioni per il verificarsi di reazioni chimiche, una delle condizioni perché si verifichi una reazione è il collisione effettiva tra le particelle. Così, l'aumento della concentrazione dei reagenti permette di avere una maggiore quantità di particelle o molecole confinate nello stesso spazio. Ciò aumenta la quantità di collisioni tra di loro e aumenta anche la probabilità che si verifichino collisioni efficaci che provocheranno la reazione. Il risultato è che la reazione avviene più velocemente.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Per vedere questo, considera il seguente esempio: quando abbiamo una brace che brucia e vogliamo che questa combustione si elabori più velocemente, soffiamo o veniamo la brace? Perché funziona?
Ebbene, uno dei reagenti in questa reazione di combustione è l'ossigeno nell'aria. Quando si scuote, la corrente d'aria rimuove la cenere che si sta formando durante la combustione e questo facilita il contatto dell'ossigeno con la brace. In questo modo aumentiamo il contatto tra i reagenti e acceleriamo la reazione di combustione.
In breve, abbiamo:

Quando si lavora con i gas, un modo per aumentare la concentrazione dei reagenti è abbassare la pressione. Quando lo facciamo, diminuiamo il volume e, di conseguenza, c'è un aumento delle concentrazioni dei reagenti.

di Jennifer Fogaça
Laureato in Chimica
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
FOGAÇA, Jennifer Rocha Vargas. "Concentrazione dei reagenti e velocità delle reazioni"; Scuola Brasile. Disponibile in: https://brasilescola.uol.com.br/quimica/concentracao-dos-reagentes-velocidade-das-reacoes.htm. Consultato il 27 giugno 2021.