Nel testo "isomero geometrico o cis-trans” è stato mostrato come l'isomerismo spaziale geometrico o cis-trans. In breve, l'isomero cis corrisponde a composti i cui ligandi uguali su ciascun atomo di carbonio sono sullo stesso piano; già nell'isomero trans, sono su lati opposti.
Questo è identificato dall'origine di questi termini, che deriva dal latino, dove cis significa "accanto a" e trans "attraverso".
Questa nomenclatura è molto utile quando due atomi di carbonio hanno ciascuno solo due diversi ligandi. Tuttavia, questi termini possono essere ambigui quando ci si riferisce agli alcheni, i cui atomi di carbonio a doppio legame hanno più di due diversi ligandi nell'insieme.
Ad esempio, considera il composto seguente:

Nota che sul carbonio X il ligando del numero atomico più basso è CH3, e sul carbonio sì è l'H Ma se dovessimo dire che questo composto è l'isomero cis, potrebbe sorgere la seguente domanda: Che tipo è cis se i gruppi di legame sono uguali (CH3) sono su lati opposti?
Pertanto, per evitare questa ambiguità, è più corretto utilizzare in questi casi la nomenclatura E-Z, dove la lettera E deriva dalla parola tedesca
entgegen, che significa “opposti” e Z deriva dalla parola tedesca zusammen, che significa "insieme". Questa nomenclatura segue la seguente regola:
Applicando questa regola di priorità al 2-clorobu-2-ene, abbiamo che nel carbonio X il ligando con il numero atomico più alto è Cl, e sul carbonio sì è il CH3. Abbiamo quindi i seguenti isomeri:
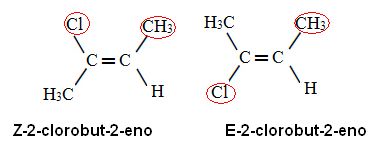
Nel primo caso i leganti con il numero atomico più alto sono dalla stessa parte del piano (Z) e nel secondo sono da parti opposte (E).
Ciò si verifica anche con composti ciclici. È importante ricordare che non è corretto mettere in relazione i termini cis e Z, e trans ed E, poiché sono sistemi di denominazione diversi.
di Jennifer Fogaça
Laureato in Chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/isomeria-e-z-no-lugar-cis-trans.htm


