Etere è una funzione organica ossigenata, cioè ha l'elemento chimico ossigeno, oltre al carbonio e all'idrogeno. Questa funzione ha come caratteristica strutturale principale la presenza di due radicali organici attaccato ad un atomo di ossigeno.
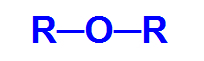
Formula strutturale generale di un etere
Quindi, la catena di carbonio di un etere è eterogenea e può avere due radicali identici o diversi, sia alchile, tipi di radicali che non hanno struttura aromatica, o arile, radicali che non hanno struttura aromatico.
Caratteristiche fisiche dell'etere
Per quanto riguarda lo stato fisico a temperatura ambiente: quando il etere ha quattro o più atomi di carbonio nella sua composizione, è liquido;
Per quanto riguarda il punto di fusione e il punto di ebollizione: rispetto ad altri composti organici di massa molare approssimativo, hanno un punto di fusione simile a quello degli alcani e inferiore al resto dei composti organico;
Per quanto riguarda la densità: sono composti che hanno una piccola densità rispetto all'acqua;
Per quanto riguarda le forze di interazione: gli eteri sono composti a bassa polarità, interagendo tra loro attraverso una debole interazione di dipolo permanente. Con l'acqua e gli alcoli, gli eteri hanno la capacità di interagire attraverso legami idrogeno.
Per quanto riguarda la polarità: sono composti che hanno geometria angolare, quindi, sono polari.
Per quanto riguarda la caratteristica organolettica: si tratta di sostanze che emanano un odore molto gradevole, ma la loro inalazione può causare dipendenza.
Nomenclatura ufficiale dell'etere
Prefisso radice minore + oxy + prefisso radice maggiore + infisso + o
Per eseguire la nomenclatura ufficiale di a etere, È fondamentale determinare qual è il tuo ligando principale e quale è il tuo ligando minore. Per fare ciò, seguire due esempi di applicazione per questa regola di denominazione di seguito:
1° Esempio:
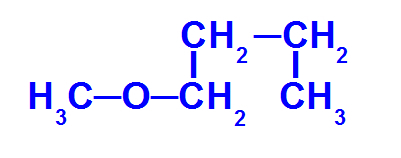
Formula di struttura di un etere con meno atomi di carbonio
L'etere sopra ha i seguenti radicali:
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
metile (CH3-);
Butile (CH3-CH2-CH2-CH2-).
Per denominare questo composto, abbiamo:
prefisso radicale minore: Met
+
ossi
+
prefisso della radice maggiore: ma
+
an (perché ha solo collegamenti singoli)
+
oh
Quindi, il nome di questo etere sarà metossibutano.
2° Esempio:
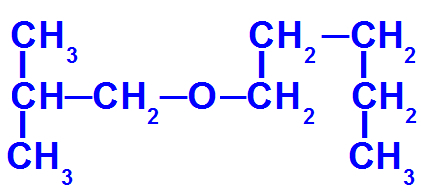
Formula di struttura di un etere con più atomi di carbonio
Questo etere ha i seguenti radicali:
isobutile [(CH3)2-CH-CH2-);
pentile (CH3-CH2-CH2-CH2-CH2).
Per nominarlo, quindi, abbiamo:
prefisso radicale minore: isobut
+
ossi
+
prefisso radice maggiore: pent
+
an (perché ha solo collegamenti singoli)
+
oh
Così, il nome di etere in questione sarà l'isobutossipentano.
Nomenclatura usuale di etere
Etere + nome dei radicali (il più semplice e poi il più complesso) + ico
o
Nomi radicali + etere
Di seguito due esempi di applicazione per questa regola di denominazione:
1° Esempio:

Formula di struttura di un etere che ha quattro atomi di carbonio
Quella etere presenta i seguenti radicali:
metile (CH3);
Isopropile (CH3-CH-CH3).
Quindi, per questo composto, abbiamo:
Etere
+
radicale minore: Metil
+
prefisso radicale maggiore: isopropyl
+
io
Così, il nome di etere in questione sarà il metilisopropil etere, oppure il metilisopropil etere.
2° Esempio:

Formula di struttura di un etere che ha cinque atomi di carbonio
L'etere sopra ha i seguenti radicali:
Etile (CH3-CH2-);
Propile (CH3-CH2-CH2-).
Per denominare questo composto, abbiamo:
Etere
+
radicale minore: etile
+
prefisso radicale maggiore: propyl
+
io
Così, il nome di etere in questione sarà l'etere etilico propilico, che può anche essere etere etilico propilico.
Usi degli eteri
In generale, gli eteri sono usati:
Come solventi organici inerti, cioè non partecipando ad alcuna reazione;
Utilizzato nell'estrazione di essenze, come fiori, legno, ecc.;
Utilizzato nell'estrazione di vari oli e grassi.
Di Me. Diogo Lopes
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
GIORNI, Diogo Lopes. "Cos'è l'etere?"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eter.htm. Consultato il 28 giugno 2021.
Chimica

Esteri, aroma alimentare, aroma, reazione di esterificazione, metil antranilato, pentil acetato, butil etanoato, etil butanoato, propanetriolo, glicerina, stearina.