doppio sale è il nome dato ad una delle classificazioni che il sali inorganici può ricevere. Le altre classificazioni sono: semplice, allume, idrossilato, idrogenato e idratato. Per essere caratterizzato come sale doppio, un sale inorganico deve avere una delle combinazioni descritte di seguito:
Un catione (Y) e due anioni qualsiasi (X e W), ed è rappresentato dalla seguente formula:
YXW
Un anione (X) e due cationi qualsiasi (Y e Z), ed è rappresentato dalla seguente formula:
YZX
Nota: Questi sali si formano quando a reazione di neutralizzazione viene eseguita tra due basi diverso e uno acido, o tra due acidi diversi e una base.
Regola di denominazione per un doppio sale
Per nominare un doppio sale, è necessario, innanzitutto, conoscerne la costituzione, perché, per ogni tipo di sale doppio, esiste una specifica regola di denominazione, come si può vedere di seguito:
a) Regola di nomenclatura per sale doppio con due cationi
Quando uno doppio sale ha due cationi, dobbiamo usare la seguente regola:

Regola di nomenclatura utilizzata per sali doppi con due cationi
Di seguito sono riportati due esempi di applicazione di questa regola di denominazione:
1° Esempio: Linea4S
Questo sale è composto da:
Anione: solfuro (S-2);
Più cationi elettropositivi: litio (Li+1);
Catone meno elettropositivo: ammonio (NH4+1).
Quindi, il suo nome è litio (doppio) solfuro di ammonio.
2° Esempio: RbCaBO3
Questo sale è composto da:
Anione: borato (BO3-3);
Più catione elettropositivo: rubidio (Rb+1);
Catone meno elettropositivo: calcio (Ca+2).
Pertanto, il suo nome è borato (doppio) di rubidio e calcio.
b) Regola di nomenclatura per sale doppio con due anioni
Quando uno doppio sale ha due anioni, dobbiamo usare la seguente regola:
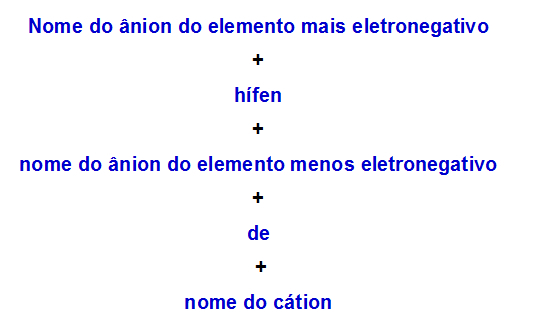
Regola di nomenclatura utilizzata per sali doppi con due anioni
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Ecco due esempi di applicazione di questa regola:
1° Esempio: MgFI
Questo sale è composto da:
Cation: magnesio (Mg+2);
Anione più elettronegativo: fluoruro (F-1);
Anione meno elettronegativo: ioduro (I-1).
Pertanto, il suo nome è fluoruro di magnesio-ioduro.
2° Esempio: ZnNO2fratello
Questo sale è composto da:
Cation: zinco (Zn+2);
Anione più elettronegativo: nitrito (NO2-1);
Anione meno elettronegativo: bromuro (Br-1).
Quindi, il suo nome è nitrito di zinco-bromuro.
Assemblaggio della formula di un doppio sale dalla sua nomenclatura
a) Per doppio sale con due cationi
La costruzione della formula di a doppio sale dipende dalla conoscenza del suo nome, che è standardizzato come in tutti i sali, cioè prima il catione e poi l'anione. Poiché il doppio sale può avere due cationi, il loro ordine e il loro posizionamento nella formula seguono il nome dato.
1° Esempio: pirofosfato di bario nichel II
Questo sale contiene fosfato (P2oh7), bario (Ba+2) e nichel II (Ni+2), cationi scritti in quella sequenza. Quindi la sua formula è BaNiP2oh7.
2° Esempio: rame II fosfato e oro I
Questo sale ha fosfato (PO4-3), rame II (Cu+2) e oro I (Au+1), cationi scritti in quella sequenza. Pertanto, la sua formula è CuAuPO4.
b) Per sale doppio con due anioni
In caso di doppio sale con due anioni, seguiamo anche, quando poniamo gli anioni nella formula, l'ordine in cui appaiono nel nome dato.
1° Esempio: nichel solfato-ioduro III
Questo sale ha anioni solfato (SO4-2) e ioduro (I-1), scritto in questa sequenza, e il catione nichel III (Ni+3). Quindi la sua formula è NiSO4IO.
2° Esempio: cianuro di piombo fosfato IV
Questo sale ha anioni fosfato (PO4-3) e cianuro (CN-1), scritto in questa sequenza, e il catione piombo IV (Pb+4). Quindi la sua formula è PbPO4CN.
Di Me. Diogo Lopes Dias
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
GIORNI, Diogo Lopes. "Cos'è un doppio sale?"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm. Consultato il 28 giugno 2021.
Nomenclatura del sale, classificazione del sale, nome dell'anione, nome del catione, solfato di ferro, solfato ferroso, nitrato di argento, cloruro di potassio, cloruro di sodio, cloruro di calcio, nitrato d'argento, solfato di rame, carbonato calcio.
Chimica

Sali di uso quotidiano, carbonato di calcio, cloruro di sodio, fluoruro di sodio, nitrato di potassio, nitrato di sodio sodio, carbonato di sodio, bicarbonato di sodio, bicarbonato di sodio, solfito di sodio, salnitro, bibita.