ITU persamaan clapeyron adalah ekspresi matematis yang menghubungkan besaran-besaran seperti tekanan (P), volume (V), suhu (T) dan jumlah partikel (n) yang membentuk a gas sempurna atau ideal. Persamaan ini dinamai fisikawan Prancis Paulusemileclapeyron dan dapat dipahami sebagai generalisasi dari hukum empiris gassempurnadiGay-Lussac, Charles dan Boyle. Itu adalah dasar untuk mempelajari gas ideal dan memungkinkan evolusi Mesin termal, membuatnya semakin efisien selama beberapa dekade terakhir.
Lihat juga: Penemuan Fisika yang Terjadi Secara Tidak Sengaja
Persamaan Clapeyron: hukum gas ideal
Persamaan Clapeyron adalah diturunkan dari tiga hukum empiris, yaitu, hukum yang ditentukan dari eksperimen from. Hukum tersebut menjelaskan perilaku gas dalam transformasi gasisovolumetrik (Hukum Gay-Lussac), isobarik (Hukum Charles) dan isoterm (Hukum Boyle). Menurut hukum-hukum ini:
dalam transformasi isovolumetrik, rasio antara tekanan dan suhu termodinamika gas ideal tetap konstan;
dalam transformasi isobarik, rasio antara volume dan suhu termodinamika gas ideal adalah konstan;
- dalam transformasi isoterm, hasil kali tekanan dan volume gas ideal tetap.
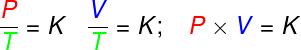
P – tekanan (Pa – pascal)
V – volume gas (m³)
T – suhu gas termodinamika (K – kelvin)
Dari ketiga hukum di atas, persamaan Clapeyron menentukan berapa nilai ini konstan (K) diperoleh pada setiap transformasi di atas. Menurut persamaan Clapeyron, konstanta ini sama dengan jumlah mol dikalikan dengan a konstanta R, yang dikenal sebagai konstanta universal gas ideal, dan sama dengan Konstanta Boltzmann dikalikan dengan Bilangan Avogadro.
Rumus
Lihat rumus yang dikenal sebagai persamaandiClapeyron:
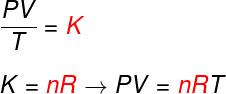
tidak - jumlah mol (mol)
R – konstanta universal gas ideal (R = 0,082 atm.l/mol. K atau 8,314 J.mol/K)
Menganalisis persamaan Clapeyron, adalah mungkin untuk melihat bahwa tekanan diberikan oleh gas ideal adalah berbanding lurus dengan suhu dan juga untuk jumlah mol. Selanjutnya, tekanan berbanding terbalik dengan volume ditempati oleh gas.
HAI model gas ideal dimungkinkan oleh persamaan Clapeyron secara luas digunakan untuk pengembangan mesin yang ditenagai oleh cairan, seperti mesin bertenaga uap dan mesin pembakaran dalam.
Beberapa hasil penting dapat diperoleh dari persamaan Clapeyron. Salah satunya, misalnya, memprediksi bahwa 1 mol gas ideal menempati volume 22.4 liter ketika mengalami tekanan sebesar 1 atm (1,01.105 Pa) dan pada suhu 273K (0 °C).
Lihat juga: Konsep Paling Penting dalam Termologi
Latihan Soal pada Persamaan Clapeyron
Pertanyaan 1 —(UECE) Suatu gas yang suhu, volume dan tekanannya dihubungkan dengan PV = nRT memiliki ciri-ciri sebagai berikut:
a) jarak rata-rata yang sangat besar antara molekul untuk mengabaikan interaksi antarmolekul, kecuali ketika bertabrakan; molekul mengalami tumbukan elastik.
b) jarak rata-rata yang sangat kecil antar molekul; molekul mengalami tumbukan tidak lenting.
c) jarak rata-rata yang sangat besar antara molekul untuk mengabaikan interaksi antarmolekul, kecuali ketika bertabrakan; molekul mengalami tumbukan tidak lenting.
d) jarak rata-rata yang sangat besar antara molekul dan dengan interaksi antarmolekul yang kuat; molekul mengalami tumbukan elastik.
Resolusi:
Dalam model gas ideal, sejumlah besar partikel tak berdimensi bergerak dengan kecepatan tinggi dalam arah acak. Satu-satunya interaksi yang dialami oleh partikel-partikel ini adalah tumbukan lenting sempurna, jadi alternatif yang tepat adalah huruf a.
Pertanyaan 2 —(UFRGS) Perhatikan pernyataan berikut tentang gas ideal.
SAYA. Konstanta R yang ada dalam persamaan keadaan untuk gas pV = nRT memiliki nilai yang sama untuk semua gas ideal.
II. Volume yang sama dari gas ideal yang berbeda, pada suhu dan tekanan yang sama, mengandung jumlah molekul yang sama.
AKU AKU AKU. Energi kinetik rata-rata molekul gas ideal berbanding lurus dengan suhu mutlak gas.
Yang mana yang benar?
a) Hanya aku
b) Hanya II
c) Hanya III
d) Hanya I dan II
e) I, II dan III
Templat:
Mari kita lihat alternatifnya:
SAYA. benar, karenanya disebut konstanta universal gas ideal.
II. benar. Menurut persamaan Clapeyron, jika dua gas ideal memiliki tekanan, suhu, dan volume yang sama, maka jumlah partikel dalam gas tersebut adalah sama.
AKU AKU AKU. benar. Menurut teorema ekuipartisi energi, energi kinetik partikel dalam gas ideal sebanding dengan suhunya.
Oleh karena itu, alternatif yang tepat adalah huruf e.
Pertanyaan 3 — (UFJF) Pria seperti Clapeyron, Boyle, Mariotte, Gay-Lussac, van der Walls, antara lain, telah mengembangkan studi penting yang melibatkan sifat-sifat gas. Perilaku gas nyata mendekati gas ideal pada kondisi tekanan rendah, serta gas yang terkandung dalam volume besar dan gas yang ditahan pada suhu tinggi. Pertimbangkan bahwa, dalam percobaan laboratorium, wadah volume V benar-benar tertutup dan berisi 1 mol gas ideal di bawah tekanan 4,0 atm mengalami pemuaian pada suhu konstan sebesar 127 C dan bahwa perilaku gas ini adalah gas ideal, seperti yang ditunjukkan pada grafis.
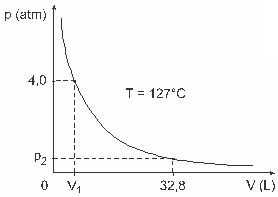
Dalam hal ini, ketika gas menempati volume yang sama dengan 32,8 L, tekanan yang diberikan olehnya adalah:
(Diberikan: konstanta universal gas sempurna adalah R = 0,082 atm. L/mol. K.)
a) 0,32 atm
b) 0,40 atm
c) 1,0 atm
d) 2,0 atm
e) 2,6 atm
Resolusi:
Huruf C
Untuk menyelesaikan latihan, kita perlu menerapkan data ke persamaan Clapeyron, tetapi sebelum itu kita perlu mengubah suhu, yang dalam derajat Celcius, ke kelvin. Periksa:

Oleh Rafael Hellerbock
guru fisika
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/fisica/a-equacao-clapeyron.htm

