Menurut Hukum Pertama Termodinamika, dalam setiap proses termodinamika jumlah panas Q diterima oleh suatu sistem sama dengan kerja yang dilakukan oleh sistem ditambah variasi energi internalnya.
Ketika tekanan konstan, panas yang dipertukarkan oleh sistem dengan media luar digunakan untuk kerja dan untuk mengubah energi dalam. Dalam banyak situasi praktis, sistem dikenai tekanan atmosfer, seperti dalam kasus reaksi kimia. Gambar di atas menunjukkan diagram PV dari jenis proses ini.
Dalam hal ini, dalam persamaan Hukum Pertama,
Q=τ+∆U
tidak ada istilah yang nol. Usaha tersebut ditulis sebagai fungsi dari variasi volume volumeV, seperti:
=P.∆V
Untuk kasus tertentu dari gas monoatomik ideal, energi dapat ditulis sebagai berikut:

Oleh karena itu, kita dapat menulis Hukum I Termodinamika sebagai fungsi dari V:


Pertukaran panas dengan medium adalah (5/2)P.ΔV, dan 40% dari total – yang sesuai dengan P.ΔV – digunakan untuk melakukan pekerjaan; dan (3/2)P.ΔV, yang setara dengan 60% dari total, digunakan untuk mengubah energi internal. Hasil ini berlaku untuk gas monoatomik ideal.
Panas terkait dengan variasi suhu (menggunakan hukum gas ideal) dengan:
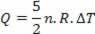
Jadi, kalor yang disuplai dapat dihitung dengan perubahan suhu atau dengan perubahan volume.
Oleh Domitiano Marques
Lulus Fisika
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/fisica/primeira-lei-para-processos-isobaricos.htm

