Dalam studi Termologi kami menyebutnya transformasi adiabatik transformasi gas di mana tidak ada pertukaran panas dengan lingkungan eksternal. Oleh karena itu, dalam transformasi adiabatik panasnya nol.
Q = 0
Jika kita menerapkan Hukum Pertama Termodinamika, kita memiliki:
Q = U+τ
U = -
Tapi apa artinya tidak ada pertukaran panas antara lingkungan eksternal? Artinya jika terjadi pemuaian gas dan gas melakukan kerja 300 J, tidak jika ada pertukaran panas dengan medium, variasi energi internal gas akan negatif, oleh karena itu, kami akan memiliki:
U = - 300 J
Sekarang, jika ada penurunan energi internal gas, kita dapat mengatakan bahwa ada juga penurunan suhu gas. Dari hukum umum gas

kita dapat mengatakan bahwa jika volume meningkat dan suhu gas menurun, tentu tekanan gas juga akan berkurang. Secara umum dapat dikatakan bahwa hal yang sama terjadi dengan kompresi, karena jika ada kompresi, energi internal gas akan meningkat, sehingga tekanan juga akan meningkat.
Peta Pikiran: Transformasi Adiabatik
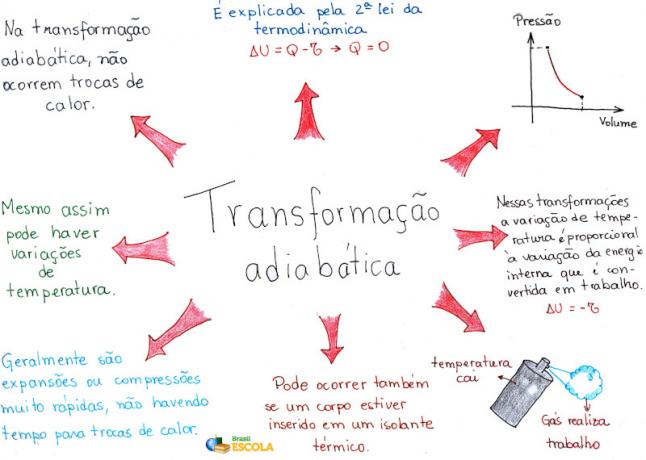
* Untuk mengunduh peta pikiran dalam PDF, Klik disini!
Secara singkat, kita dapat mengatakan bahwa:
- dalam ekspansi adiabatik, penurunan suhu dan tekanan;
- dalam kompresi adiabatik, suhu dan tekanan meningkat.
Bagan di bawah ini memberikan gambaran umum tentang transformasi adiabatik:
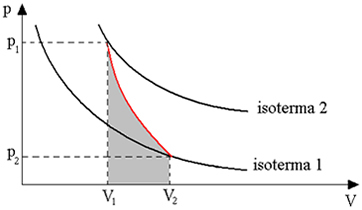
Transformasi adiabatik diperoleh dengan menggunakan wadah yang diisolasi secara termal, atau juga melalui kompresi atau ekspansi yang sangat cepat.
Dengan demikian, kita dapat menyimpulkan bahwa ketika gas bertukar panas dengan lingkungan eksternal, dibutuhkan beberapa waktu untuk panas menyebar melalui massa gas dan untuk mencapai keseimbangan. Oleh karena itu, ketika ekspansi dan kompresi cepat dilakukan, praktis tidak ada pertukaran panas dengan lingkungan eksternal.
* Peta Pikiran oleh Saya. Rafael Helerbrock
Oleh Domitiano Marques
Lulus Fisika
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/fisica/estudo-transformacao-adiabatica.htm

