garam anorganik mereka dibentuk oleh asosiasi ionik dari setidaknya satu kation (dibentuk oleh logam apa pun atau oleh amonium) dan anion (sederhana atau senyawa).
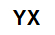
Rumus molekul umum garam
Ketika ditambahkan ke air, garam terdisosiasi, melepaskan setidaknya satu kation selain hidronium (H+) dan anion selain hidroksida (OH-).
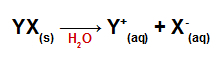
Persamaan disosiasi untuk setiap garam
Klasifikasi garam
Garam, secara umum, dapat memiliki klasifikasi berikut:
garam sederhana: garam yang dibentuk oleh hanya satu kation dan satu anion. Contoh: NaCl, CaSO4, KCN, NH4BERSAMA3 dll.
garam terhidrogenasi: ia memiliki dua kation (salah satunya harus hidronium) dan sebuah anion. Contoh: NaHCO3, CaHBO3 dll.
Garam hidroksil: ia memiliki kation dan dua anion (salah satunya harus hidroksida). Contoh: MgOHCl, Al(OH)2ClO3 dll.
garam terhidrasi: menyajikan molekul air yang terkait dengan struktur kristalnya. Contoh: CaCl2.2H2O, CuSO4.6H2dll.
garam ganda: ia memiliki dua kation (semua berbeda dari hidronium) dan satu anion atau satu kation dan dua anion (semua berbeda dari hidroksida). Contoh: Jenis4CN, AgFeBO3 dll.
Tawas: adalah garam yang dibentuk oleh dua sulfat dengan kation NOx sama dengan +1 dan +3, ditambah 24 molekul air. Contoh: Ag2HANYA4.Al2(HANYA4)3.24H2pada suatu2HANYA4.Sb2(HANYA4)3.24H2HAI
Aturan penamaan garam
Nama anion + de + nama kation
→ K3DEBU4
Garam memiliki anion fosfat (PO4-3) dan kation kalium (K+1), maka namanya adalah kalium fosfat.
→ Kasus3
Garam memiliki anion sulfit (SO3-2) dan kation kalsium (Ca+2), maka namanya adalah kalsium sulfit.
CATATAN: Jika kation tersebut bukan perak, seng atau unsur yang termasuk dalam famili IA, IIA dan IIIA, kita harus menunjukkan NOX-nya dengan angka romawi di depan nama kation.
→ Cu2HANYA4
Garam memiliki anion sulfat (SO4-2) dan kation kalsium (Cu+1), maka namanya adalah tembaga sulfat I.
garam terhidrogenasi: Untuk garam ini, sebelum nama anion, kita harus menulis awalan yang mengacu pada jumlah hidrogen dalam rumus. Awalan ini harus terpisah dari kata hidrogen oleh tanda hubung.
→ NaHCO3
Garam memiliki hidrogen, anion karbonat dan kation natrium, sehingga namanya adalah natrium monohidrogen karbonat.
Garam hidroksil: Untuk garam ini, sebelum nama anion, kita harus menulis awalan yang mengacu pada jumlah hidroksil dalam rumus. Awalan ini harus terpisah dari kata hidroksi oleh tanda hubung.
→ Al(OH)2ClO3
Garam memiliki dua hidroksil, anion klorat dan kation aluminium, jadi namanya adalah aluminium dihidroksi-klorat.
garam terhidrasi: Untuk garam ini, setelah nama kation, kita harus menulis awalan yang mengacu pada jumlah molekul air dalam rumus. Awalan ini harus terpisah dari kata terhidrasi oleh tanda hubung.
→ CaCl2.2H2HAI
Garam memiliki dua molekul air, anion klorida dan kation kalsium, sehingga namanya adalah kalsium klorida dihidrat.
Garam ganda dengan dua kation: Untuk garam ini, kita harus menulis kata rangkap dalam tanda kurung setelah nama anion dan kemudian nama kation yang paling elektropositif dan kation lainnya.
→ AgFeBO3
Garam ini memiliki kation perak (lebih elektropositif) dan besi II, selain anion borat. Namanya borat (ganda) dari perak dan besi II.
-
Garam ganda dengan dua anion:
Nama anion paling elektronegatif + tanda hubung + nama anion paling elektronegatif + de + nama kation
→ Tipe4CN
Garam ini mengandung kation titanium IV, selain fosfat (anion yang lebih elektronegatif) dan anion sianida. Namanya titanium sianida fosfat IV.
garam tawas: Untuk garam ini, kami mengabaikan aturan umum. Tulis saja istilah tawas diikuti dengan nama kation muatan +3 dan nama kation muatan +1, dipisahkan dengan kata penghubung e.
→ Dalam2HANYA4.Sb2(HANYA4)3.24H2HAI
Garam tawas memiliki kation antimon +3 dan kation natrium +1, sehingga namanya adalah tawas dan natrium antimon III.
Sifat fisik garam
Mereka padat pada suhu kamar;
Mereka memiliki titik leleh dan titik didih yang tinggi;
Mereka terbentuk dari ikatan ionik;
Mereka menghantarkan arus listrik dalam keadaan cair (setelah mengalami fusi) atau ketika dilarutkan dalam air;
Secara umum, mereka larut dalam air, tetapi ada garam yang dianggap praktis tidak larut.
Sifat kimia garam
Garam adalah senyawa yang mempunyai kemampuan untuk bereaksi secara kimia (asalkan tidak memiliki kation atau anion yang sama dengan zat lain) dengan beberapa golongan zat, yaitu:
Dalam reaksi pertukaran ganda dengan asam: mereka membentuk garam baru dan asam baru.
Dalam reaksi pertukaran ganda dengan basa: mereka membentuk garam baru dan basa baru.
Di sebuah reaksi pertukaran ganda dengan garam lain: membentuk dua garam baru.
Beberapa garam memiliki kemampuan untuk menderita penguraian ketika mengalami panas, membentuk dua atau lebih zat baru. Jika kita memanaskan natrium bikarbonat (NaHCO3), misalnya akan terurai, membentuk natrium karbonat (Na2BERSAMA3), air (H2O) dan karbon dioksida (CO2).
Oleh Saya Diogo Lopes Dias
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-sais-inorganicos.htm
