ITU auto-oxi-reduksi atau reaksi yang tidak proporsional adalah jenis reaksi redoks di mana unsur kimia yang sama mengalami oksidasi dan pengurangan. Mari kita lihat dua contoh jenis reaksi ini dan cara menyetarakannya menggunakan metode redoks:
Contoh 1:
PADA2- + H+ → TIDAK3- + TIDAK + H2HAI
- Dengan menghitung bilangan oksidasi (NOX) dari semua atom dan ion yang terlibat dalam reaksi, dimungkinkan untuk memverifikasi siapa yang teroksidasi dan siapa yang bereaksi:
+3 -2 +1 +5 -2 +2 -2 +1 -2
PADA2- + H+ → TIDAK3- + TIDAK + H2HAI
- Perhatikan bahwa nitrogen adalah spesies yang bereaksi dan teroksidasi:
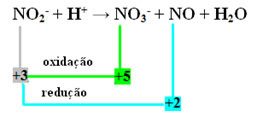
- Untuk melakukan penyeimbangan redoks dari reaksi ini, kita harus menghubungkan NOX dengan produk, bukan reaktan:
PADA3- =∆Nox = 5 - 3 = 2
TIDAK=∆Nox = 3 - 2 = 1
- Membalikkan NOX dengan koefisien, kita mendapatkan:
PADA3- =∆NOX= 2 → 2 akan menjadi koefisien NO
TIDAK=∆NOX= 1→ 1 akan menjadi koefisien NO3-
PADA2- + H+ → 1 PADA3- + 2 TIDAK + H2HAI
- Dengan ini, kita sudah tahu bahwa ada 3 N dalam produk, jadi koefisien NO2- akan menjadi 3:
3 TIDAK2- + H+ → 1 TIDAK3- + 2 TIDAK + H2HAI
- Untuk menentukan koefisien H+ dan dari H2O, ingatlah bahwa jumlah elektron yang diterima sama dengan jumlah elektron yang disumbangkan; dengan demikian, muatan reagen akan sama dengan muatan produk. Dengan cara ini, kita dapat membuat skema berikut:
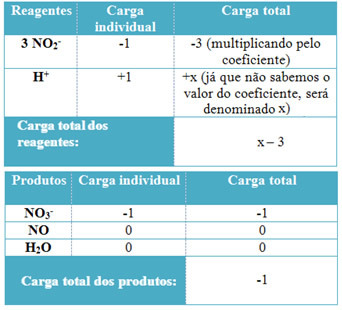
Berdasarkan informasi ini, kita mendapatkan bahwa total muatan reagen sama dengan x – 3 dan produknya sama dengan -1. Seperti yang dinyatakan, muatan keduanya harus sama. Karena kita sudah memiliki total beban produk, kita dapat melakukan perhitungan sederhana untuk mengetahui berapa nilai x:
x -3 = -1
x = -1 +3
x = 2
Jadi, koefisien H+ adalah 2 dan, akibatnya, H2akan menjadi 1:
3 TIDAK2- + 2 H+ → 1 TIDAK3- + 2 TIDAK + 1 H2HAI
Contoh ke-2:
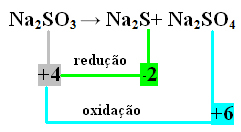
Dalam hal ini, S yang mengalami reduksi dan oksidasi secara bersamaan. Jadi, seperti yang telah dilakukan sebelumnya, kita dapat menghubungkan NOX dengan produk dan membalikkan nilainya, menetapkan koefisiennya:
Di2 S=∆Nox = 4 - (-2) = 6 → 6 akan menjadi koefisien Na2 HANYA4
Di2 HANYA4=∆Nox = 6 - 4 = 2 → 2 akan menjadi koefisien Na2 s
Di2 HANYA3→ 2 Di2 Y+ 6 Di2 HANYA4
Karena ada 8 belerang di cabang ke-2, koefisien Na2 HANYA3 akan menjadi 8:
8 In2 HANYA3→ 2 In2 S + 6 In2 HANYA4
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/reacoes-auto-oxirreducao.htm

