Satu reaksi adisi adalah proses kimia di mana atom dari zat anorganik ditambahkan ke molekul organik, yang harus memiliki salah satu karakteristik berikut:
Struktur terbuka yang mengandung pengikatan atau tautan pi;
Struktur tertutup jenuh (hanya dengan tautan sigma);
Struktur tak jenuh tertutup (dengan pi atau ikatan aromatik).
Senyawa organik yang memiliki ciri-ciri tersebut adalah sebagai berikut: Hidrokarbon:
alkena;
Alkuna;
Alkadiena;
Cyclans;
Siklus;
Aromatik.
Selama reaksi adisi, satu atau lebih ikatan pi, atau ikatan sigma (dalam kasus eksklusif cyclan) terputus menyebabkan dua atau lebih valensi bebas muncul (situs ikatan) pada karbon yang terlibat, seperti pada contoh di bawah:
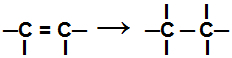
Pemutusan ikatan pi pada alkena
Setelah ikatan ini diputus, penambahan atom harus terjadi di tempat ikatan baru yang dibuat dalam senyawa organik. Kami daftar di bawah ini jenis reaksi adisi yang dapat dilakukan dengan senyawa organik.
hidrogenasi
Di dalam reaksi adisi, selain senyawa organik, reaktan lainnya adalah gas hidrogen (H
2). Di setiap karbon, di mana fisi terjadi (pemutusan ikatan sigma atau pi, seperti yang terlihat sebelumnya), akan ada ikatan atom hidrogen yang mengacu pada jumlah ikatan yang terputus.Ketika kita melakukan hidrogenasi siklobutana, misalnya, ikatan sigma terputus antara karbon 1 dan 2. Kemudian, atom hidrogen mengikat masing-masing karbon ini:
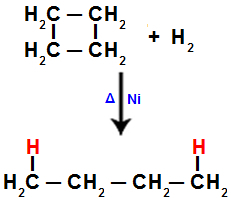
Persamaan yang mewakili hidrogenasi dalam siklobutana
Halogenasi
Selain senyawa organik, reagen lain dalam ini reaksi adisi adalah halogen molekuler (gas klorin-Cl2, gas fluor-F2, yodium padat-I2 dan brom cair-Br2). Pada setiap karbon, di mana fisi terjadi (pemutusan ikatan sigma atau pi, seperti yang terlihat di atas), akan ada ikatan atom dari halogen mengacu pada jumlah koneksi yang rusak.
Jadi, ketika kita melakukan halogenasi (menggunakan gas klorin) dari siklopropena, ikatan pi terputus antara karbon 1 dan 2. Kemudian, atom klorin mengikat masing-masing karbon ini:

Persamaan yang mewakili halogenasi dalam siklopropena
Reaksi adisi dengan halida
Halida adalah asam hydra anorganik, dibentuk oleh atom hidrogen dan atom hidrogen. halogen, seperti asam klorida (HCl), asam fluorida (HF), asam hidrobromat (HBr), asam hidroiodik (HI).
Di reaksi adisi dengan halida, selain senyawa organik, reagen lainnya adalah halida, maka salah satu karbon, di mana pemotongan (pemutusan ikatan sigma atau pi, seperti yang terlihat di atas), harus menerima atom hidrogen, dan yang lainnya menerima halida.
Menurut Aturan Markovnikov, atom karbon yang paling terhidrogenasi (atau karbon yang terikat pada radikal yang lebih kecil) harus menerima hidrogen, dan karbon yang kurang terhidrogenasi (atau karbon yang terikat pada radikal yang lebih besar) harus menerima halida.
Misalnya, ketika kita melakukan reaksi ini pada propena dengan asam klorida (HCl), ikatan pi terputus antara karbon 1 dan 2. Kemudian, hidrogen mengikat karbon 1 (lebih terhidrogenasi) dan klorin ke karbon 2 (kurang terhidrogenasi):
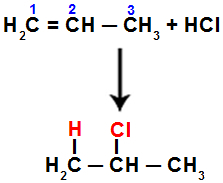
Persamaan yang mewakili adisi dengan halida dalam propena
Reaksi hidrasi
Molekul air, ketika terionisasi, menghasilkan kation hidronium (H+) dan anion hidroksida (OH-). Untuk alasan itu, dalam hal ini reaksi adisi, selain senyawa organik, reaktan lainnya adalah air. Jadi, salah satu karbon, di mana fisi terjadi (pemutusan ikatan sigma atau pi, seperti yang terlihat di atas), menerima kation hidronium, dan yang lainnya menerima anion hidroksida.
Menurut aturan Markovnikov, atom karbon yang paling terhidrogenasi (atau karbon yang terikat pada radikal yang lebih kecil) harus menerima hidronium, dan karbon yang kurang terhidrogenasi (atau karbon yang terikat pada radikal yang lebih besar) harus menerima hidroksida.
Ketika kita menghidrasi penta-1,4 diena, misalnya, ikatan pi terputus antara karbon 1 dan 2, dan antara karbon 4 dan 5. Kemudian, karbon 1 dan 5 menerima hidronium, dan karbon 2 dan 4 menerima hidroksida:
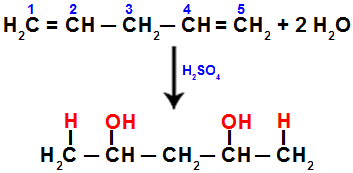
Persamaan yang mewakili adisi dengan hidrasi dalam penta-1,4 diena
Oleh Saya Diogo Lopes Dias
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-reacao-adicao.htm
