unsur kimia fosfor (P) termasuk dalam periode ketiga dari Tabel Periodik dan keluarga Nitrogen (VA). Untuk alasan ini, atomnya biasanya membuat tiga ikatan kimia untuk mencapai teori oktet (stabilitas). Namun, ada beberapa situasi di mana atom fosfor membuat lebih dari tiga ikatan, fakta yang hanya mungkin melalui fenomena hibridisasi.
Untuk memahami hibridisasi fosfor, pertama-tama kita harus memahami mengapa atom unsur ini membuat tiga ikatan. Untuk melakukan ini, kami hanya perlu memantau distribusi elektronik Anda:

Distribusi Fosfor Elektronik
Kita dapat mengamati bahwa, pada lapisan valensi, atom fosfor memiliki sublevel 3s yang lengkap (dengan dua elektron) dan sublevel 3p yang tidak lengkap (masing-masing dari tiga orbital sublevel p memiliki elektron). Di bawah ini kita memiliki distribusi elektron dalam orbital dari sublevel Lapisan valensi fosfor:
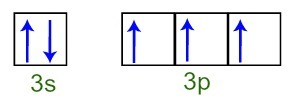
Representasi elektron kulit valensi atom fosfor
Karena masing-masing orbital sublevel 3p tidak lengkap, atom fosfor mampu membuat tiga ikatan kimia, sehingga mencapai stabilitas.
Sekarang ketika kita melihat substansi PCl5, misalnya, kami yakin bahwa, dalam molekul ini, fosfor mengalami hibridisasi, karena membuat lima sambungan. Karena klorin, yang termasuk dalam keluarga VIIA, membutuhkan ikatan agar stabil dan molekulnya memiliki lima atom ini unsur, masing-masing harus membuat ikatan, yang membuat atom fosfor, pada gilirannya, juga harus membuat lima Koneksi. Kejadian ini hanya mungkin melalui through hibridisasi (penyatuan orbital atom yang tidak lengkap) dari fosfor.
Saat menerima energi dari lingkungan luar, elektron atom Fosfor menjadi tereksitasi. Segera setelah itu, salah satu dari dua elektron yang termasuk dalam sublevel 3s pindah ke orbital kosong yang ada di sublevel d, yang sampai saat itu tidak memiliki elektron. Lihat diagram di bawah ini:
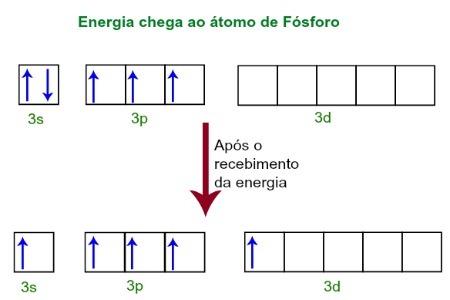
Setelah menerima energi, elektron fosfor tereksitasi dan satu menempati orbital dari sublevel d.
Pada saat ini, kita memiliki di lapisan valensi Fosfor sebuah orbital s, tiga orbital p dan orbital d yang tidak lengkap.Pada akhirnya, kelima orbital ini berhibridisasi, yaitu bergabung, menghasilkan lima orbital atom yang tidak lengkap, yang sekarang mampu membuat lima ikatan kimia.

Hibridisasi orbital atom fosfor yang tidak lengkap
Sebagai orbital s, tiga orbital p dan orbital d bergabung, hibridisasi Fosfor adalah jenis sp3d.
Oleh Saya Diogo Lopes Dias
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/hibridizacao-fosforo.htm

