Ikatan kovalen terjadi ketika dua atom berbagi pasangan elektron untuk memperoleh konfigurasi elektron dari suatu gas mulia (dengan 8 elektron di kulit valensi atau dengan 2, dalam kasus yang hanya memiliki kulit K), menurut aturan oktet.
Namun, ada kasus khusus ikatan kovalen di mana: pasangan elektron bersama hanya berasal dari salah satu atom yang sudah stabil. Sebelumnya, jenis ikatan kovalen ini disebut datif, hari ini lebih sering disebut koordinat.
Lihat beberapa contoh untuk memahami bagaimana ini terjadi:
- CO (karbon monoksida):
Karbon memiliki 4 elektron di kulit valensinya. Oleh karena itu, menurut aturan oktet, agar stabil, perlu menerima 4 elektron lagi, berjumlah 8. Oksigen, di sisi lain, memiliki 6 elektron di kulit valensi dan perlu menerima 2 elektron untuk mendapatkan konfigurasi neon gas mulia.
Jadi, pertama, karbon dan oksigen berbagi dua pasang elektron sehingga oksigen stabil:
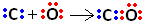
Namun, karbon tetap tidak stabil karena masih memiliki 6 elektron dan membutuhkan 2. Oleh karena itu, oksigen, yang sudah stabil, berbagi salah satu pasangan elektronnya dengan karbon, yaitu membuat ikatan datif dengannya, membuatnya stabil:

Perhatikan bahwa ikatan kovalen koordinat dapat dilambangkan dengan tanda hubung, sama seperti ikatan kovalen biasa.
- HANYA2 (Sulfur dioksida):
Setiap atom belerang dan oksigen memiliki 6 elektron di kulit valensinya, sehingga masing-masing harus menerima 2 elektron. Awalnya, belerang membuat dua ikatan kovalen umum, berbagi dua pasang elektron dengan salah satu atom oksigen, keduanya tetap stabil dengan 8 elektron.
Tapi, atom oksigen lainnya tidak stabil, jadi belerang berbagi sepasang elektron dengannya melalui ikatan kovalen terkoordinasi atau datif:
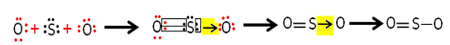
Perhatikan bahwa dalam hal ini kita memiliki tiga atom dalam molekul, sehingga dapat terjadi perpindahan ikatan dari satu atom ke atom lainnya. Molekul belerang dioksida juga dapat direpresentasikan seperti ini: O S O.
Kami menyebut fenomena ikatan ini resonansi. Lihat tiga contoh lagi dalam tabel di bawah ini:
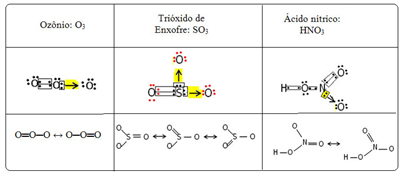
Struktur yang mungkin disebut struktur resonansi atau bentuk kanonik.
Jenis ikatan ini juga terjadi pada pembentukan ion, seperti pada kasus ion hidronium (H3HAI+) dan amonium (NH4+).
Pertama, kation H+ itu terbentuk ketika hidrogen kehilangan satu elektronnya, meninggalkannya dengan muatan positif. Jadi perlu menerima dua elektron agar stabil. Ini terjadi melalui ikatan datif dengan air (dalam kasus ion hidronium) dan dengan amonia (dalam kasus ion amonium). Menonton:

Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/ligacao-covalente-dativa-ou-coordenada.htm
