Asam dan basa adalah dua jenis zat korosif, namun dianggap berlawanan secara kimiawi.
Salah satu perbedaan terbesar antara asam dan basa adalah basa, jika bersentuhan dengan larutan berair, melepaskan ion negatif, hidroksil (OH-). Asam, dalam kontak dengan air, melepaskan ion hidrogen positif (H+).
Zat apa pun dengan nilai pH antara 0 hingga 7 dianggap asam, sedangkan nilai pH 7 hingga 14 adalah basa. Nilai 7 adalah netral, yang sesuai dengan air.
| Asam | Basis | |
|---|---|---|
| Definisi Arrhenius | Asam adalah senyawa kimia apa pun yang, dalam larutan berair, melepaskan ion hidrogen (H+). |
Basa, atau alkali, adalah zat yang, dalam larutan berair, melepaskan hidroksil, ion negatif (OH-) |
| Definisi Bronsted-Lowry | Asam adalah zat yang menyumbangkan proton. | Basa adalah zat apa pun yang menerima proton. |
| definisi lewis | Selama ikatan kimia, asam adalah asam yang menerima pasangan elektron. | Dalam ikatan kimia, basa adalah yang menyumbangkan pasangan elektron. |
| nilai pH | Kurang dari 7,0. | Lebih besar dari 7.0. |
| Karakter fisik | Asam dapat terjadi dalam bentuk padat, cair atau gas, tergantung pada suhunya. | Seringkali padat kecuali amonia yang merupakan gas. |
| Struktur | Asam bersifat molekuler, yaitu dibentuk oleh ikatan kovalen di mana elektron digunakan bersama. | Basa dapat bersifat ionik atau molekuler. |
| rumus kimia | Asam memiliki rumus kimia dengan H di awal, misalnya HCl (asam klorida). Pengecualian adalah asam asetat (cuka), dengan CH3COOH. | Basa memiliki OH di akhir rumusnya, misalnya NaOH (natrium hidroksida). |
| Kelarutan dalam air | Mereka cenderung cukup larut dalam air. | Sebagian besar basa praktis tidak larut. |
| Reaksi pada indikator Phenolphthalein | Itu tetap tidak berwarna. | Buat larutan menjadi merah muda. |
| Tes Ph (dengan kertas lakmus) | Itu berubah menjadi merah. | Itu berubah menjadi biru. |
| konduktivitas listrik | Mereka hanya menghantarkan listrik ketika dilarutkan dalam air. | Mereka juga melakukan arus listrik dalam larutan air. |
| Contoh | Asam asetat, asam sulfat. | Natrium hidroksida, amonia |
Apa itu asam dan basa
Asam adalah senyawa ionik yang bila dilarutkan dalam air menghasilkan ion hidrogen positif (H+). Sebaliknya, basa adalah senyawa ionik yang membentuk ion hidroksida bermuatan negatif (OH-) dalam air.
Definisi ini, yang dibuat oleh ilmuwan Swedia Svante Arrhenius, adalah yang paling banyak digunakan untuk mengklasifikasikan asam dan basa, namun ada definisi lain.
Definisi yang diberikan oleh Johannes N. Bronsted dan Thomas Lowry, yang dikenal sebagai definisi proton, mengatakan bahwa asam adalah zat yang menyumbangkan proton, sedangkan basa adalah zat yang menerima proton.
Dalam definisi yang diberikan oleh Gilbert Newton Lewis dari Amerika Utara, asam adalah zat yang menerima pasangan elektron dalam ikatan kimia, sedangkan basa memberikan pasangan elektron.
pH asam dan basa
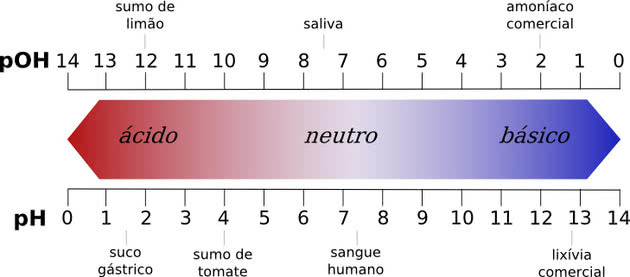
Semua senyawa kimia memiliki nilai pH, yang dapat berkisar dari 0 hingga 14, dimana angka tersebut mewakili konsentrasi ion hidrogen dalam suatu larutan.
PH netral adalah pH air murni, yaitu 7. Zat apa pun dengan nilai pH antara 0 hingga 7 dianggap asam, sedangkan nilai pH 7 hingga 14 adalah basa.
Semakin rendah asamnya di bawah 7,0, semakin kuat. Pada basa, semakin tinggi nilai pH maka akan semakin kuat.
Karakteristik Asam:
- Rasanya pahit;
- Dapat membakar kulit saat disentuh;
- Dapat menimbulkan korosi pada logam dan kulit;
- Membuat kertas lakmus merah;
- Dalam indikator universal diidentifikasi dengan warna merah atau oranye.
Karakteristik Basis
- Rasa zat;
- Saat menyentuh, Anda merasakan sesuatu yang kental;
- Banyak basa bereaksi dengan asam dan menghasilkan garam;
- Basa kuat dapat bereaksi hebat dengan asam;
- Basa mengubah kertas lakmus menjadi biru;
Indikator asam dan basa
Indikator pH, atau indikator asam-basa, adalah zat yang digunakan untuk mengetahui apakah suatu larutan adalah asam atau basa.
Hal ini dimungkinkan karena sifat fisika-kimianya yang memiliki kemampuan berubah warna sesuai pH zat uji.
Di antara banyak indikator buatan yang digunakan di laboratorium, yang paling terkenal adalah fenolftalein, kertas lakmus, dan indikator universal.
- Phenolphthalein tetap tidak berwarna jika terkena asam, dan berubah menjadi merah muda jika terkena basa.
- Kertas lakmus menjadi biru dengan basa dan merah dengan asam.
- Indikator universal adalah indikator asam-basa yang paling akurat karena menunjukkan warna yang berbeda sesuai dengan masing-masing nilai pH.

Aplikasi asam dan basa dalam kehidupan sehari-hari
Asam sering digunakan untuk menghilangkan karat dari logam, sebagai elektrolit dalam baterai, untuk memproses mineral, untuk menghasilkan pupuk dan bensin, dan sebagai bahan tambahan dalam makanan dan minuman.
Basa terutama digunakan dalam pembersihan, seperti deterjen pencuci piring dan sabun cuci, pembersih oven, dan penghilang noda.