Ilmuwan Friedrich Kohlrausch (1840-1910) adalah orang pertama yang mengusulkan bahwa air murni menghantarkan listrik, meskipun dalam skala kecil. Ini karena air berperilaku secara amfoter; yaitu, pada kesempatan tertentu ia bertindak seperti asam, menyumbangkan proton (H+); dan yang lain berperilaku seperti basa, menerima proton.
Ini berarti bahwa air melakukan ionisasinya sendiri, menurut persamaan kimia yang ditunjukkan di bawah ini:
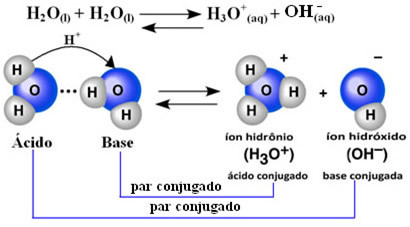
Proses ini disebut autoionisasi air dan itu terjadi dalam skala yang sangat kecil, yaitu, air adalah elektrolit yang sangat lemah, dengan nilai derajat ionisasi yang rendah dan konstanta ionisasi pada kesetimbangan (Kç). Inilah mengapa air memiliki konduktivitas yang rendah.
Untuk mendapatkan gambaran, pada suhu sekitar 25°C dimungkinkan untuk menentukan bahwa konsentrasi ion hidroksida dan hidronium yang dihasilkan dalam ionisasi sendiri air murni adalah sama dengan 1. 10-7 mol L-1. Ini berarti bahwa dari satu miliar molekul air, hanya dua yang terionisasi.
Konstanta keseimbangan ionik air disebut çkonstanta disosiasi air,konstanta autoprotolisisatau produk ionik air.Konstanta ini diwakili oleh Kw, karena w mengacu pada kata air, yang dalam bahasa Inggris berarti air.
Perhitungannya dilakukan dengan cara yang sama seperti konstanta kesetimbangan lainnya, mengingat bahwa, seperti yang dinyatakan dalam teks "Konstanta Setarakan Kc dan Kp”, dalam hal ini, hanya produk yang akan muncul dalam ekspresi, karena air dalam keadaan cair memiliki aktivitas yang sama ke 1. Zat cair atau padat murni tidak dimasukkan ke dalam ekspresi konstanta disosiasi karena mereka tidak berubah. Hanya larutan berair dan gas yang ditempatkan. Jadi kita punya:
Kw = [H3HAI+]. [oh-]
Kw = (1. 10-7). (1. 10-7)
Kw = 10-14
Seperti konstanta kesetimbangan lainnya, baikw itu hanya berubah dengan perubahan suhu. Ketika suhu air meningkat, ionisasinya juga meningkat, yang berarti bahwa ionisasi diri air adalah proses endotermik, yaitu menyerap panas.
Hal ini dapat dilihat pada nilai produk ionik air (Kw) diberikan dalam tabel di bawah ini pada suhu yang berbeda:
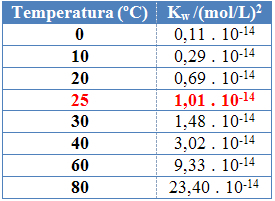
Produk ionik air akan selalu memiliki nilai tetap pada setiap suhu, baik dalam air murni maupun dalam larutan. Bahkan jika larutan memiliki konsentrasi ion H H3HAI+ dan oh- berbeda, produk di antara mereka akan tetap konstan.
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/produto-ionico-Agua-kw.htm



