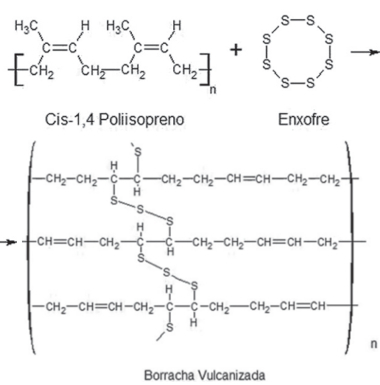
ITU isomerisme itu adalah fenomena yang diamati ketika senyawa yang berbeda dibentuk oleh jumlah yang sama dari jenis atom yang sama.
Oleh karena itu, kita dapat menemukan zat kimia dengan rumus molekul yang sama dan rumus struktur atau susunan ruang yang berbeda.
Fenomena ini banyak diamati dalam Kimia Organik, yang mempelajari senyawa karbon. Karena setiap atom unsur ini dapat membuat 4 ikatan kimia, dimungkinkan untuk mengamati kombinasi yang berbeda.
Karena perubahan susunan atom menimbulkan zat baru, akibatnya, mereka memiliki sifat fisik dan kimia yang berbeda.
Ketika kita mengatakan senyawa mana yang isomer berarti bahwa mereka memiliki bagian yang sama, karena kata tersebut merupakan kombinasi dari dua istilah yang berasal dari bahasa Yunani: iso, berarti "benar-benar", dan belaka, yang merupakan "bagian".
Dua kelompok utama isomerisme adalah bidang dan ruang (stereoisomerisme).
ITU isomerisme datar itu dapat divisualisasikan dengan rumus struktur datar senyawa dan memiliki lima kelas: posisi, fungsi, rantai, kompensasi dan tautomer.
ITU isomerisme ruang itu diamati oleh orientasi senyawa dan dibagi menjadi geometris (cis-trans) dan optik.
Konsep isomerisme diperkenalkan pada tahun 1830 oleh ilmuwan Swedia Jacob Berzelius.
Contoh isomer
ITU isomerisme rantai itu terjadi ketika set atom yang sama terhubung untuk membentuk struktur dari kelompok fungsional yang sama, tetapi dengan rantai yang berbeda.
Contoh: rumus molekul C4H10 hidrokarbon dapat berbentuk lurus atau bercabang.

ITU isomerisme posisi terjadi ketika senyawa dibentuk oleh gugus fungsi yang sama, tetapi mereka berada pada posisi yang berbeda dalam rantai.
Contoh: Rumus molekul C4H9OH sesuai dengan dua jenis alkohol.
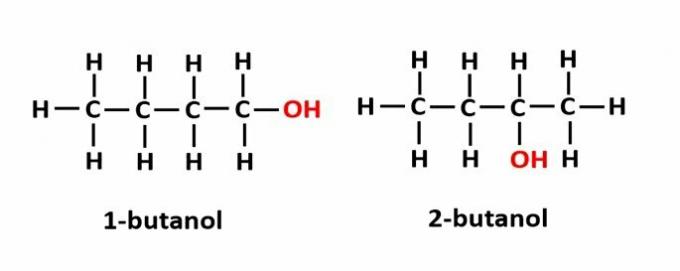
ITU fungsi isomerisme terjadi ketika rumus molekul yang sama sesuai dengan dua senyawa dengan gugus fungsi yang berbeda.
Contoh: Rumus molekul C2H6O sesuai dengan dua isomer yang memiliki fungsi alkohol (-OH) dan eter (-O-).
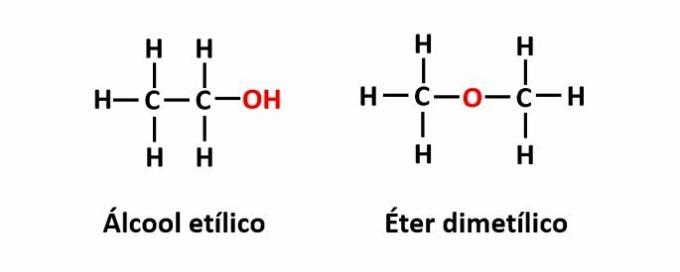
ITU isomerisme kompensasi itu terjadi ketika ada heteroatom dalam rantai dan menempati posisi yang berbeda. Ini adalah kasus khusus dari isomerisme posisi.
Contoh: Rumus molekul C4H10The menunjukkan adanya atom oksigen dalam rantai, tetapi posisinya dapat berubah dan membentuk senyawa yang berbeda.
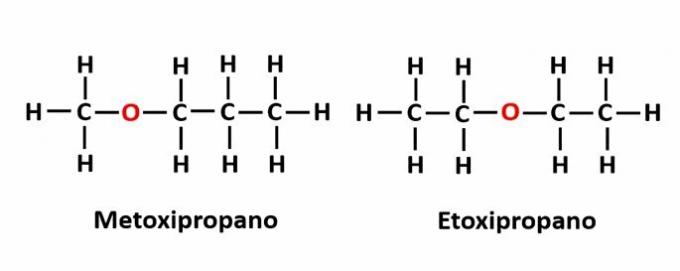
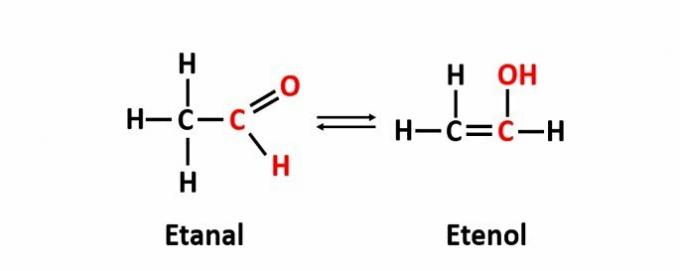
ITU isomerisme dinamis, juga disebut tautomer, terjadi ketika dua senyawa dengan fungsi yang berbeda berada dalam larutan yang sama dalam kesetimbangan dinamis. Ini adalah kasus khusus dari isomerisme fungsi.
Contoh: Rumus molekul C2H4O sesuai dengan senyawa dengan fungsi aldehida dan enol.
Belajar lebih tentang isomerisme datar.
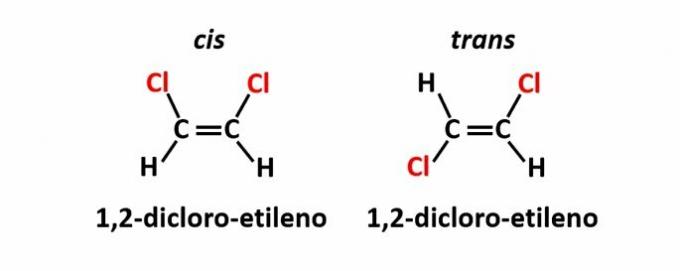
ITU isomerisme geometris, juga disebut isomer cis-trans, terjadi ketika adanya ikatan rangkap atau struktur siklik menyebabkan ligan yang sama berada pada sisi bidang yang sama (cis) atau pada sisi yang berlawanan (trans).
Contoh: atom klor dalam senyawa dengan rumus molekul C2H2Cl2 mereka mungkin memiliki dua struktur spasial.
ITU isomerisme optik terjadi ketika, ketika membelokkan cahaya terpolarisasi yang dipancarkan pada struktur, senyawa berhasil membelokkan sinar bercahaya ke kiri, jika merupakan isomer levorotatory (l), atau ke kanan, jika merupakan isomer dextrorotatory (D).
Contoh: Jenis isomerisme ini terjadi dengan asam laktat. Perhatikan di bawah bahwa gambar spektral dari isomer tidak tumpang tindih, maka mereka disebut enansiomer.
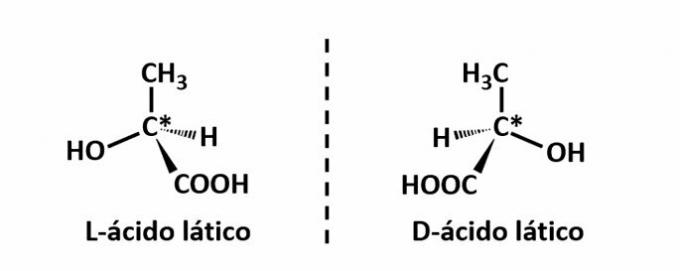
Simbol C* menunjukkan adanya karbon kiral dalam struktur ini, yaitu atom karbon dengan 4 penghubung yang berbeda.
Pelajari lebih lanjut tentang isomerisme dengan isi:
- Jenis isomerisme
- isomer ruang
- isomer geometris
- isomer optik
- Latihan isomerisme bidang