Reaksi dari tambahan adalah tindakan penting sehubungan dengan sintesis organik, karena melalui mereka sejumlah zat organik yang menarik dapat dikembangkan.
Agar reaksi adisi terjadi, perlu untuk membuat dua situs pengikatan dalam rantai karbon, yang terjadi hanya ketika rantai tidak jenuh (adanya tautan pi). Jadi, ketika tautan pi terputus, situs muncul dalam rantai.
Sekelompok zat yang dapat digunakan selain sintesis adalah sikloalkana atau cyclans, kelompok hidrokarbon dengan rantai siklik dan jenuh. Mereka lolos dari aturan umum penjumlahan karena mereka tidak memiliki tautan pi, tetapi tergantung pada beberapa kondisi (panas, logam katalis, medium asam) mereka dapat mengalami pemutusan rantai antara dua atom karbon, menyebabkan dua situs pengikatan muncul untuk penambahan berlangsung. Namun, ada fakta yang membatasi penggunaan senyawa ini. Faktanya adalah panggilan teori tegangan cincin, diusulkan oleh Adolf V. Bayer pada tahun 1885.
Agar ikatan sigma antara karbon diputus, harus ada ketidakstabilan tertentu antara karbon. Ketidakstabilan ini terkait dengan sudut ikatan antar karbon. Menurut Bayer, sudut yang memberikan a
stabilitas yang hebat untuk tautan sigma adalah 109,47HAI. Jadi, rantai yang memiliki sudut antar karbon lebih kecil dari 109,47HAI mereka cenderung memiliki ketidakstabilan dalam ikatan sigma antara karbon yang membentuk rantai, yang mendukung kerusakan mereka yang bersekutu dengan kondisi eksternal yang ideal.Satu-satunya sikloalkana yang memiliki sudut lebih kecil dari 109,47HAI di antara karbonnya adalah siklopropana (60HAI), siklobutana (90HAI) dan siklopentana (108HAI). Siklopentana memiliki sudut yang sangat dekat dengan 109,47HAI ia memiliki ikatan sigma yang sangat stabil, oleh karena itu ia tidak dapat mengalami reaksi adisi apa pun. Di bawah ini kita memiliki struktur ketiga sikloalkana ini:

Rumus struktur siklopropana, siklobutana dan siklopentana, masing-masing
Pengamatan: Setiap sikloalkana yang memiliki lebih dari 5 karbon dalam rantai akan melakukan reaksi substitusi untuk contoh, dan tidak pernah penambahan karena ikatan sigma antara atom karbonnya sangat stabil.
Reaksi adisi yang dapat terjadi dengan sikloalkana pada dasarnya semua, tetapi dengan siklopentana satu-satunya yang dapat terjadi adalah hidrogenasi dan halogenasi. Di bawah ini adalah contoh adisi dengan sikloalkana dan kondisi kemunculannya:
a) Hidrogenasi
Reaksi sikloalkana dengan molekul hidrogen dengan adanya katalis logam bubuk (seng, nikel atau platinum) dengan adanya pemanasan (sekitar 180°CHAIC). Dalam reaksi ini, sikloalkana akan menghasilkan a alkana. Dalam reaksi ini, setelah siklus terputus, satu atom hidrogen ditambahkan ke setiap karbon dari ikatan sigma yang terputus.

Reaksi adisi dalam siklobutana menggunakan hidrogen
b) Halogenasi
Reaksi sikloalkana dengan molekul halogen (klorin, brom, yodium, misalnya) dengan adanya katalis besi III klorida (FeCl3). Dalam reaksi ini, sikloalkana akan menghasilkan a halida organik dengan dua atom halogen dalam rantai. Setelah siklus terputus, kami memiliki penambahan atom halogen pada masing-masing karbon dari ikatan sigma yang terputus.

Reaksi adisi dalam siklobutana menggunakan bromin
c) Reaksi dengan Halogenhidrida (asam halida)
Reaksi sikloalkana dengan molekul hidrat anorganik yang mengandung halogen (HCl. HBr, HI). Karena asam digunakan sebagai reaktan, katalis tidak digunakan. Dalam reaksi ini, sikloalkana akan menghasilkan a halida organik dengan hanya satu atom halogen dalam rantai. Setelah siklus terputus, kita memiliki penambahan atom hidrogen pada salah satu karbon dari ikatan sigma yang terputus dan sebuah halogen pada karbon lainnya. Mematuhi aturan Markovnikov (H pada karbon terhidrogenasi paling banyak dan halogen pada karbon terhidrogenasi paling sedikit).
Catatan: Ini hanya terjadi dengan siklopropana dan siklobutana.
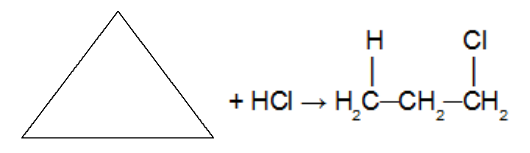
Reaksi adisi dalam siklopropana menggunakan asam klorida
Catatan: Ini hanya terjadi dengan siklopropana dan siklobutana.
d) Hidrasi
Reaksi sikloalkana dengan molekul air dengan adanya asam sulfat dan pemanasan. Dalam reaksi ini, sikloalkana akan menghasilkan a alkohol tunggal (alkohol dengan hanya satu gugus OH dalam rantai). Setelah siklus terputus, kita memiliki penambahan atom hidrogen pada salah satu karbon dari ikatan sigma yang terputus dan hidroksil (OH) pada karbon lainnya. Mematuhi aturan Markovnikov (H pada karbon terhidrogenasi paling banyak dan hidroksil pada karbon terhidrogenasi paling sedikit).
Catatan: Ini hanya terjadi dengan siklopropana dan siklobutana.

Reaksi adisi dalam siklopropana menggunakan asam klorida
Oleh Saya Diogo Lopes Dias
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/adicoes-ciclanos.htm
