Di antara gaya antarmolekul, gaya dipol yang diinduksi dipol yang diinduksi mereka adalah satu-satunya yang tidak dipelajari oleh fisikawan Belanda Johannes Diederik Van der Waals (1837-1923). Mereka dijelaskan oleh fisikawan Jerman Fritz Wolfgang London (1900-1954), sehingga gaya ini juga disebut pasukan london atau kekuatan dispersi london. Nama lain yang diberikan untuk kekuatan ini adalah dipol yang diinduksi dipol sesaat.
Gaya semacam ini terjadi di zat non polar, seperti H2, O2, F2, Cl2, CO2, CH4 dan C2H6, antara lain. Dan mereka juga dapat terjadi antara atom gas mulia, ketika mereka mendekat, menyebabkan tolakan antara elektrosfer mereka. Dengan cara ini, elektron menumpuk di sisi tertentu, yang terpolarisasi negatif dan sisi yang berlawanan secara positif, karena kekurangan muatan negatif.
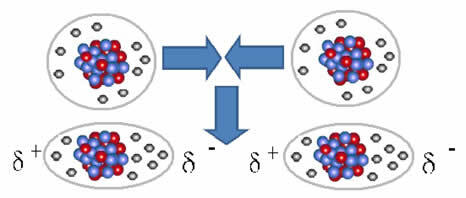
Molekul nonpolar dapat berubah dari keadaan gas - di mana mereka sangat berjauhan dan tidak ada interaksi, karena tidak ada kutub - ke keadaan cair dan padat. Dalam keadaan agregasi ini, molekul-molekulnya lebih dekat dan gaya tarik-menarik elektronik atau tolakan antara elektronnya dan inti dapat menyebabkan deformasi awan elektronik mereka, sesaat, yang berasal dari kutub positif dan negatif sementara.
Dipol sesaat dapat menginduksi polarisasi molekul tetangga, menghasilkan gaya tarik menarik.
Induksi ini juga dapat terjadi. antara molekul yang berbeda dan umumnya kekuatan ini lebih lemah dalam intensitas daripada kekuatan ikatan dipol-dipol dan hidrogen. Oleh karena itu, padatan dengan kekuatan interaksi ini seperti es kering (karbon dioksida - CO2) dan yodium (I2), yang berada dalam wujud padat, bersifat sublim (menjadi gas); karena energi yang dibutuhkan untuk mengganggu interaksi mereka kecil.
Contoh gaya antarmolekul antara molekul polar dan nonpolar terjadi antara gas oksigen (nonpolar) dan air (polar). Ternyata ujung negatif air mendekati O2, menolak dirinya sendiri, dan dengan demikian awan elektronik dari molekul non-polar bergerak menjauh. Oksigen kemudian terpolarisasi sesaat dan mulai berinteraksi dengan air, larut di dalamnya.
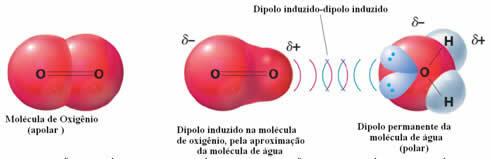
Karena gaya-gaya ini lemah, kelarutan gas ini dalam air kecil. Meski begitu, keberadaannya sangat penting untuk melestarikan kehidupan berbagai organisme akuatik.
Gaya interaksi ini juga terjadi di alam, memberikan kepatuhan antara cakar tokek dan permukaan tempat mereka berjalan. Itu sebabnya mereka bisa berjalan di dinding dan langit-langit tanpa jatuh atau menempel.
Oleh Jennifer Fogaa
Lulus kimia
Tim Sekolah Brasil
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/forcas-dipolo-induzido-dipolo-induzido-ou-dispersao-london.htm

