Isomerisme kimia adalah fenomena yang diamati ketika dua atau lebih zat organik memiliki rumus molekul yang sama, tetapi struktur dan sifat molekulnya berbeda.
Zat kimia dengan karakteristik ini disebut isomer.
Istilah ini berasal dari kata Yunani iso = sama dan hanya = bagian, yaitu bagian yang sama.
Ada beberapa jenis isomerisme:
- isomer datar: Senyawa diidentifikasi dengan rumus struktur datar. Ini dibagi menjadi isomerisme rantai, isomerisme fungsi, isomerisme posisi, isomerisme kompensasi dan isomerisme tautomerisme.
- isomer ruang: Struktur molekul senyawa memiliki struktur spasial yang berbeda. Ini dibagi menjadi isomerisme geometris dan optik.
isomer datar
Di isomerisme datar atau isomerisme konstitusional, struktur molekul zat organik adalah datar.
Senyawa yang menunjukkan karakteristik ini disebut isomer datar.
isomer rantai
Isomerisme rantai terjadi ketika atom karbon memiliki rantai yang berbeda dan fungsi kimia yang sama.
Contoh:
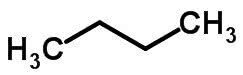
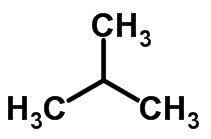
Fungsi Isomerisme
Isomerisme fungsi terjadi ketika dua atau lebih senyawa memiliki fungsi kimia yang berbeda dan rumus molekul yang sama.
Contoh: Kasus ini umum terjadi antara aldehida dan keton.
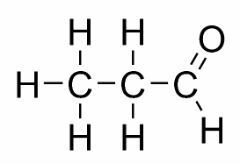
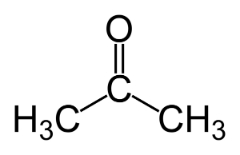
isomer posisi
Isomerisme posisi terjadi ketika senyawa dibedakan oleh ketidakjenuhan, percabangan, atau posisi gugus fungsi yang berbeda dalam rantai karbon. Dalam hal ini, isomer memiliki fungsi kimia yang sama.
Contoh:

isomer penyeimbang
Kompensasi isomerisme atau metamerisme terjadi pada senyawa dengan fungsi kimia yang sama yang berbeda dengan posisi heteroatom.
Contoh:

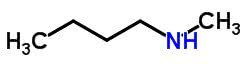
Tautomeri
Tautomerisme atau isomerisme dinamis dapat dianggap sebagai kasus spesifik dari isomerisme fungsi. Dalam hal ini, satu isomer dapat berubah menjadi yang lain dengan mengubah posisi elemen dalam rantai.
Contoh:

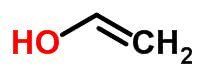
isomer ruang
ITU isomerisme ruang, juga disebut stereoisomerisme, terjadi ketika dua senyawa memiliki rumus molekul yang sama dan rumus struktur yang berbeda.
Dalam jenis isomerisme ini, atom didistribusikan dengan cara yang sama, tetapi menempati posisi yang berbeda dalam ruang.
isomer geometris
ITU isomerisme geometrik atau cis-trans terjadi pada rantai terbuka tak jenuh dan juga pada senyawa siklik. Untuk melakukan ini, ligan karbon harus berbeda.

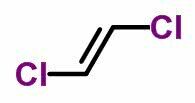
- Ketika ligan yang sama berada di sisi yang sama, nomenklatur isomer menerima awalan cis.
- Ketika ligan yang sama berada di sisi yang berlawanan, nomenklatur menerima awalan trans.
IUPAC (International Union of Pure and Applied Chemistry) merekomendasikan bahwa alih-alih cis dan trans, huruf Z dan E digunakan sebagai awalan.
Ini karena Z adalah huruf pertama dari kata Jerman zusammen, yang berarti "bersama". Dan itu huruf pertama dari kata Jerman semangat, yang berarti "berlawanan".
isomer optik
ITU isomerisme optik ditunjukkan oleh senyawa yang aktif secara optik. Itu terjadi ketika suatu zat disebabkan oleh penyimpangan sudut dalam bidang cahaya terpolarisasi.
- Benda yang membelokkan cahaya optik ke kanan disebut Pengguna tangan kanan.
- Ketika suatu zat membelokkan cahaya optik ke kiri, zat tersebut disebut levorotary.
Suatu zat juga bisa ada dalam dua bentuk yang aktif secara optik, dextogyra dan levogyra. Dalam hal ini disebut enansiomer.
Agar senyawa karbon aktif secara optik, ia harus kiral. Ini berarti bahwa ligan mereka tidak dapat tumpang tindih, menjadi asimetris.
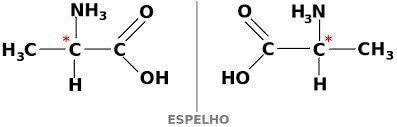
Sebaliknya, jika suatu senyawa memiliki bentuk dekstrogira dan levorotary di bagian yang sama, mereka disebut campuran rasemat. Aktivitas optik campuran rasemat tidak aktif.
Baca juga:
- Karbon
- Kimia organik
- Formula molekul
- Formula struktural
Latihan
1. (Mackenzie 2012) Nomor kolom B, yang berisi senyawa organik, mengasosiasikannya dengan kolom A, sesuai dengan jenis isomerisme yang disajikan setiap molekul organik.
kolom A
1. isomer penyeimbang
2. isomer geometris
3. isomer rantai
4. isomer optik
Kolom B
( ) siklopropana
( ) etoksi-etana
( ) bromo-kloro-fluoro-metana
( ) 1,2-dikloro-etena
Urutan angka yang benar pada kolom B dari atas ke bawah adalah
a) 2 - 1 - 4 - 3.
b) 3 - 1 - 4 - 2.
c) 1 - 2 - 3 - 4.
d) 3 - 4 - 1 - 2.
e) 4 - 1 - 3 - 2.
Alternatif b) 3 - 1 - 4 - 2.
2. (Uerj) Isomer adalah fenomena yang dicirikan oleh fakta bahwa rumus molekul yang sama mewakili struktur yang berbeda.
Mempertimbangkan isomerisme struktural datar untuk rumus molekul C4H8, kita dapat mengidentifikasi isomer dari jenis berikut:
a) rantai dan posisi
b) rantai dan fungsi
c) fungsi dan kompensasi
d) posisi dan kompensasi
Alternatif a) senar dan posisi
3. (OSEC) Propanon dan isopropenol merupakan contoh kasus Isomerisme:
a) dari metameria
b) fungsi
c) tautomer
d) cis-trans
e) rantai
Alternatif c) dari tautomer
Lihat juga: Latihan Isomerisme Datar


