Tabel periodik adalah alat studi penting yang mengumpulkan informasi tentang semua unsur kimia yang diketahui.
Uji pengetahuan Anda dengan daftar ini 17 pertanyaan dengan pendekatan yang berbeda pada subjek dan selesaikan keraguan Anda dengan resolusi yang dikomentari setelah umpan balik.
Untuk membantu memahami pertanyaan, gunakan use tabel periodik lengkap dan diperbarui.
Organisasi Tabel Periodik
pertanyaan 1
(UFU) Pada awal abad kesembilan belas, dengan penemuan dan isolasi berbagai unsur kimia, menjadi penting untuk mengklasifikasikan mereka secara rasional, untuk melakukan studi sistematis. Banyak kontribusi ditambahkan hingga mencapai klasifikasi periodik unsur kimia saat ini. Mengenai klasifikasi periodik saat ini, jawablah:
a) Bagaimana unsur-unsur terdaftar secara berurutan dalam tabel periodik?
Tabel periodik disusun menjadi urutan unsur-unsur kimia dalam urutan nomor atom. Jumlah ini sesuai dengan jumlah proton dalam inti atom.
Metode pengorganisasian ini diusulkan oleh Henry Moseley ketika dia mengkonfigurasi ulang tabel yang diusulkan oleh Dmitri Mendeleiev.
Sebuah elemen dapat ditempatkan di tabel dengan keluarga dan periode di mana elemen itu dimasukkan. Distribusi ini terjadi sebagai berikut:
| kelompok atau keluarga | 18 urutan vertikal |
| Kumpulan dari unsur-unsur yang memiliki kesamaan sifat. |
| Periode | 7 urutan horizontal |
| Jumlah lapisan elektronik yang dimiliki elemen. |
b) Golongan apa dalam tabel periodik yang dapat ditemukan: halogen, logam alkali, logam alkali tanah, kalkogen, dan gas mulia?
Pengelompokan unsur ke dalam golongan dilakukan menurut sifat-sifatnya. Unsur-unsur yang berada dalam kelompok yang sama memiliki karakteristik yang sama dan untuk klasifikasi yang diberikan kita harus:
| Klasifikasi | Kelompok | Keluarga | Elemen |
| halogen | 17 | 7A | F, Cl, Br, I, At dan Ts |
| logam alkali | 1 | 1A | Li, Na, K, Rb, Cs dan Fr |
| logam alkali tanah | 2 | 2A | Be, Mg, Ca, Sr, Ba dan Ra |
| kalkogen | 16 | 6A | O, S, Se, Te, Po dan Lv |
| gas mulia | 18 | 8A | Dia, Ne, Ar, Kr, Xe, Rn dan Og |
pertanyaan 2
(PUC-SP) Selesaikan masalah berdasarkan analisis pernyataan di bawah ini.
I – Tabel periodik modern saat ini disusun dalam urutan menaik dari massa atom.
II - Semua unsur yang memiliki 1 elektron dan 2 elektron pada kulit valensi adalah, masing-masing, logam alkali dan logam alkali tanah, asalkan bilangan kuantum utama dari lapisan ini (n 1).
III - Pada periode yang sama, elemen-elemen menyajikan jumlah level (lapisan) yang sama.
IV - Dalam kelompok yang sama (keluarga), elemen memiliki jumlah level (lapisan) yang sama.
Disimpulkan bahwa, sehubungan dengan tabel periodik unsur kimia saat ini, mereka benar:
a) I dan IV (hanya).
b) I dan II (hanya).
c) II dan III (hanya).
d) II dan IV (hanya).
e) III dan IV (hanya).
Alternatif yang benar: c) II dan III (hanya).
Menganalisis setiap alternatif kita harus:
AKU SALAH. Unsur-unsur disusun menurut urutan nomor atomnya.
II – BENAR. Elektron pada kulit valensi menentukan golongan tempat unsur tersebut berada.
| logam alkali | 1 elektron pada kulit valensi |
| 3Baca | 2-1 |
| 11Di | 2-8-1 |
| 19K | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87Fr | 2-8-18-32-18-8-1 |
| logam alkali tanah | 2 elektron pada kulit valensi |
| 4menjadi | 2-2 |
| 12mg | 2-8-2 |
| 20Sini | 2-8-8-2 |
| 38Bapak | 2-8-18-8-2 |
| 56ba | 2-8-18-18-8-2 |
| 88Katak | 2-8-18-32-18-8-2 |
Bilangan kuantum utama sesuai dengan kulit tempat elektron berada, berbeda dari 1 karena dengan distribusi elektronik kita perhatikan bahwa lokasi elektron adalah dari kulit kedua atau n=2.
III – BENAR. Letak suatu unsur dalam periode tertentu disebabkan oleh banyaknya lapisan pada saat melakukan distribusi elektronik.
| Periode | 7 urutan horizontal |
| periode pertama | 1 lapisan: K |
| periode ke-2 | 2 lapisan: K, L |
| periode ke-3 | 3 lapisan: K, L, M |
| periode ke-4 | 4 lapisan: K, L, M, N |
| periode ke-5 | 5 lapisan: K, L, M, N, O |
| periode ke-6 | 6 lapisan: K, L, M, N, O, P |
| periode ke-7 | 7 lapisan: K, L, M, N, O, P, Q |
Contoh: unsur kimia yang terletak pada periode kedua.
IV – SALAH. Unsur-unsur yang termasuk dalam kelompok yang sama memiliki karakteristik yang sama dan ini disebabkan oleh fakta bahwa mereka memiliki jumlah elektron yang sama di kulit valensi.
Contoh:
| Berilium | Magnesium |
|
2 elektron dalam lapisan valensi. |
2 elektron dalam lapisan valensi. |
Oleh karena itu, berilium dan magnesium adalah bagian dari golongan 2 Tabel Periodik.
pertanyaan 3
(Unitin) Mengenai klasifikasi periodik unsur modern, tentukan pernyataan yang benar:
a) dalam satu keluarga, unsur-unsur umumnya memiliki jumlah elektron yang sama di kulit terakhir.
b) pada tabel periodik, unsur-unsur kimia ditempatkan dalam urutan massa atom.
c) dalam satu keluarga, unsur-unsur memiliki sifat kimia yang sangat berbeda.
d) dalam satu periode, unsur-unsur memiliki sifat kimia yang sama.
e) semua unsur yang mewakili termasuk dalam golongan B dari tabel periodik.
Alternatif yang benar: a) dalam satu keluarga, unsur-unsur umumnya memiliki jumlah elektron yang sama pada kulit terakhir.
a) BENAR. Unsur-unsur kimia dari keluarga yang sama memiliki jumlah elektron yang sama di kulit terakhir dan ini membuat mereka memiliki karakteristik yang serupa.
b) SALAH. Massa atom bertambah dengan bertambahnya nomor atom unsur.
c) SALAH. Sifat kimia unsur-unsurnya serupa, sehingga mereka dikelompokkan dalam keluarga yang sama.
d) SALAH. Pada suatu waktu, unsur-unsur memiliki elektron yang terdistribusi dalam jumlah kulit yang sama.
e) SALAH. Elemen perwakilan milik grup A, yang sesuai dengan keluarga: 1A, 2A, 3A, 4A, 5A, 6A, 7A dan 8A. Unsur yang termasuk golongan B adalah unsur transisi.
pertanyaan 4
(Vunesp) Mengingat sifat-sifat unsur kimia dan tabel periodik, tidak benar untuk menyatakan:
a) logam adalah zat yang menghantarkan arus listrik, bersifat ulet dan dapat ditempa.
b) bukan logam adalah zat yang tidak dapat menghantarkan arus listrik, tidak ulet, atau dapat ditempa.
c) semimetal memiliki penampilan fisik seperti logam, tetapi perilaku kimianya mirip dengan non-logam.
d) sebagian besar unsur kimia terbuat dari non-logam.
e) gas mulia bersifat monoatomik.
Alternatif yang salah: d) sebagian besar unsur kimia adalah non-logam.
Perhatikan klasifikasi unsur kimia pada tabel periodik menjadi logam, nonlogam, dan semilogam.

Seperti yang kita lihat, sebagian besar unsur adalah logam.
a) BENAR. Logam menghantarkan listrik karena awan elektron yang dibentuk oleh elektron bebas, yang merupakan karakteristik strukturnya. Mereka ulet karena dapat berubah menjadi kabel atau lembaran, tergantung pada daerah di mana tekanan diterapkan. Mereka juga dapat ditempa, karena lembaran yang sangat tipis dapat diproduksi dengan bahan jenis ini.
b) BENAR. Nonlogam memiliki karakteristik yang berlawanan dengan logam. Alih-alih konduktor, mereka adalah isolator termal yang baik dan, karena rapuh, mereka tidak dicetak menjadi kabel atau lembaran karena tidak memiliki keuletan dan kelenturan yang baik.
c) BENAR. Semilogam memiliki sifat-sifat antara logam dan nonlogam. Menjadi semikonduktor listrik, mereka memiliki kilau logam tetapi rapuh seperti non-logam.
d) SALAH. Sebagian besar unsur diklasifikasikan sebagai logam. Kelas-kelas logam yang ada dalam tabel periodik adalah: alkali, alkali tanah, transisi internal dan eksternal.
e) BENAR. Gas mulia bersifat monoatomik, sehingga hanya diwakili oleh inisialnya.
Contoh:
| gas mulia | kalkogen |
| Helium (Dia) | Oksigen (O2) |
| monoatomik: dibentuk oleh atom | diatomik: dibentuk oleh dua atom |
Karena stabilitas gas mulia, unsur-unsur keluarga ini memiliki reaktivitas rendah dan juga dikenal sebagai inert.
pertanyaan 5
Tentang organisasi Tabel Periodik saat ini, jawablah:
a) Apa itu kolom?
b. Apa saja garis-garisnya?
c. Bagaimana cara mengorganisasikan unsur-unsur kimia?
Jawaban:
a) kolom adalah kelompok dari Tabel Periodik, sebelumnya disebut keluarga, yang menyatukan unsur-unsur kimia dengan sifat yang sama.
b) Garis adalah periode dari Tabel Periodik dan menunjukkan jumlah lapisan elektronik atom dalam keadaan dasar.
c) Unsur-unsur kimia dalam Tabel Periodik saat ini disusun dalam urutan menaik dari nomor atom, yang menunjukkan jumlah proton dalam inti atom.
Keluarga Tabel Periodik
pertanyaan 1
(CESGRANRIO) Membuat hubungan antara kolom di bawah ini, yang sesuai dengan keluarga unsur menurut tabel periodik, urutan numeriknya adalah:
| 1. gas mulia | • Grup 1A |
| 2. logam alkali | • Grup 2A |
| 3. logam alkali tanah | • Grup 6A |
| 4. Kalkogen | • Grup 7A |
| 5. halogen | • Grup 0 |
a.1, 2, 3, 4, 5.
b) 2, 3, 4, 5, 1.
c) 3, 2, 5, 4, 1.
d) 3, 2, 4, 5, 1.
e) 5, 2, 4, 3, 1.
Alternatif yang benar: b) 2, 3, 4, 5, 1.
| kelompok | konfigurasi elektronik |
| • Grup 1A: 2. logam alkali | kami1 (dengan n |
| • Grup 2A: 3. logam alkali tanah | kami2 (dengan n |
| • Grup 6A: 4. Kalkogen | kami2np4 |
| • Grup 7A: 5. halogen | kami2np5 |
| • Grup 0: 1. gas mulia | 1 detik2 (Dia) atau kita2np6 (jika n > 1) |
pertanyaan 2
(UECE) Unsur kimia dengan Z = 54 memiliki konfigurasi 5s di lapisan valensinya2 5p6. Unsur-unsur dengan Z = 52 dan dengan Z = 56 termasuk dalam famili:
a) kalkogen dan alkali tanah
b.halogen dan basa
c. halogen dan alkali tanah
d.kalkogen dan alkali
Alternatif yang benar: a) kalkogen dan alkali tanah.
Mengingat nomor atom, kami melakukan distribusi elektronik dan menemukan hasil berikut:
| 54X dan | 52Kamu | 56ba |
|
8 elektron dalam lapisan valensi |
6 elektron dalam lapisan valensi |
2 elektron dalam lapisan valensi |
| Gas Mulia: keluarga 8A | Kalkogen: keluarga 6A | Alkaline Earth: keluarga 2A |
pertanyaan 3
(F. Ibero-Americana-SP) Kelompok Tabel Periodik yang dicirikan oleh dominasi unsur buatan adalah sebagai berikut:
a) lantanida
b.gas mulia
c.logam transisi
d.logam alkali tanah
e) aktinida
Alternatif yang benar: e) aktinida.
Unsur buatan adalah unsur yang tidak ada di alam dan telah disintesis di laboratorium melalui reaksi nuklir.
Mereka juga disebut elemen transuranik, karena elemen radioaktif ini memiliki nomor atom lebih besar dari 92, yang sesuai dengan uranium.
Secara umum, elemen-elemen ini berumur pendek, bertahan hingga sepersekian detik.
Menurut informasi ini kita harus:
Unsur-unsur yang terdapat di alam adalah: lantanida, gas mulia, logam transisi dan logam alkali tanah. Dengan pengecualian teknesium dan prometium, yang buatan.
Dominasi unsur buatan adalah aktinida, diklasifikasikan sebagai logam transisi internal dan dimasukkan dalam tabel periodik di bawah lantanida. Dari seri itu, hanya aktinium, thorium, protaktinium dan uranium yang alami.
pertanyaan 4
(U. Gereja Katolik Salvador-BA) Spesies X2- dengan 8 elektron pada kulit terluar (kulit valensi) dapat berasal dari unsur X, yang dalam Tabel Periodik termasuk golongan:
a) 7A
b) 6A
c) 2A
d) 1A
e) 8A
Alternatif yang benar: b) 6A.
Menurut aturan oktet, agar suatu unsur memperoleh stabilitas, ia mengasumsikan konfigurasi elektronik gas mulia, yang memiliki 8 elektron di kulit valensi.
Muatan 2- pada spesies X2- menunjukkan bahwa unsur tersebut telah memperoleh 2 elektron.
Konfigurasi elektron spesi yang memiliki 8 elektron pada kulit terluar adalah ns2np6.
Setelah kehilangan dua elektron, elemen kembali ke keadaan dasarnya dengan konfigurasi elektron ns2np4.
Keenam elektron dalam kulit valensi adalah karakteristik dari kalkogen, unsur-unsur dari keluarga 6A.
Sebagai contoh:
| Elemen: oksigen | konfigurasi elektronik |
| 8HAI | 1 detik22 detik22p4 |
| spesies O2- | 1 detik22 detik22p6 |
Belajar lebih tentang Keluarga Tabel Periodik.
unsur kimia
pertanyaan 1
(CESGRANRIO) Mengingat unsur nomor atom 3, 9, 11, 12, 20, 37, 38, 47, 55, 56 dan 75, opsi yang hanya mengandung logam alkali adalah:
a) 3, 11, 37 dan 55
b) 3, 9, 37 dan 55
c) 9, 11, 38 dan 55
d) 12, 20, 38 dan 56
e) 12, 37, 47 dan 75
Alternatif yang benar: a) 3, 11, 37 dan 55
Logam alkali sesuai dengan unsur kimia yang mengakhiri distribusi elektronik dengan elektron di sublevel s.
Membuat distribusi elektronik dari nomor atom yang diberikan, kami memiliki logam alkali berikut:
| Z = 3 | Z = 11 | Z = 37 | Z = 55 |
| Litium | Sodium | rubidium | sesium |
Nomor atom lainnya sesuai dengan unsur-unsur dari kelompok berikut:
Logam alkali tanah: mengakhiri distribusi elektronik pada sublevel s2.
| Z = 12 | Z = 38 | Z = 56 |
| Magnesium | Stronsium | Barium |
Logam transisi: mengakhiri distribusi elektronik pada sublevel d.
| Z = 30 | Z = 47 | Z = 75 |
| Seng | Perak | renium |
Halogen: mengakhiri distribusi elektronik pada sublevel p5.
| Z = 9 |
pertanyaan 2
(Unirio) “Jantung buatan yang ditempatkan di Eloi mulai dikembangkan empat tahun lalu di Amerika Serikat dan sudah digunakan oleh sekitar 500 orang. Set, yang disebut Heartmate, terdiri dari tiga bagian utama. Yang paling penting adalah tas bundar seberat empat pon, berdiameter 12 sentimeter dan tebal 3 sentimeter, terbuat dari titanium — logam putih-perak, ringan dan kuat.” Majalah Veja, Juli 1999.
Di antara logam di bawah ini, yang memiliki, pada lapisan terakhir, jumlah elektron yang sama dengan titanium adalah:
a) C
tempat sampah
c) Ga
d) mg
e) Xe
Alternatif yang benar: d) Mg.
| Titanium | konfigurasi elektronik | Distribusi lapisan |
| 22Kamu | 1 detik2 2 detik2 2p6 3 detik2 3p6 4s2 3d2 | 2, 8, 10, 2 |
Dari distribusi elektronik titanium, kita melihat bahwa unsur ini memiliki 2 elektron di kulit terakhir.
| Elemen | konfigurasi elektronik | Distribusi lapisan |
| 6Ç | 1 detik2 2 detik2 2p2 | 2, 4 |
| 11Di | 1 detik2 2 detik2 2p6 3 detik1 | 2, 8, 1 |
| 31ga | 1 detik2 2 detik2 2p6 3 detik2 3p6 4s2 3d104p1 | 2, 8, 18, 3 |
| 12mg | 1 detik2 2 detik2 2p6 3 detik2 | 2, 8, 2 |
| 54X dan | 1 detik2 2 detik2 2p6 3 detik2 3p6 3d10 4s2 4p6 4d10 5 detik2 5p6 | 2, 8, 18, 18, 8 |
Unsur yang juga memiliki 2 elektron pada kulit terakhir adalah magnesium.
pertanyaan 3
(UFPA) Pertimbangkan elemen kimia tertentu yang sublevel paling energiknya adalah 5s2. Nomor atom dan golongannya pada Tabel Periodik berturut-turut adalah:
a) 20; 1A
b) 20; 2A
c) 38; 2A
d) 38; 1A
e) 39; 2A
Alternatif yang benar: c) 38; 2A
Dengan melakukan distribusi elektronik, kami menemukan bahwa:
- Unsur kimia terletak di keluarga 2A, karena memiliki sublevel paling energik s2
- Memiliki nomor atom 38, yang sesuai dengan jumlah total elektron yang didistribusikan.
- Itu terletak di periode kelima, karena distribusi elektronik dilakukan hingga lapisan kelima.
Memeriksa informasi ini dalam Tabel Periodik, kita dapat memastikan bahwa itu adalah elemen strontium.
pertanyaan 4
(UFC) Sebuah atom x memiliki satu proton lebih banyak daripada atom y. Berdasarkan informasi tersebut, tentukan pernyataan yang benar.
a) Jika y adalah alkali tanah, x adalah logam alkali.
b) Jika y adalah gas mulia, x adalah halogen.
c) Jika y adalah logam transisi, x adalah gas mulia.
d) Jika y adalah gas mulia, x adalah logam alkali.
e) x terletak pada periode yang sama sebelum atom y dalam tabel periodik.
Alternatif yang benar: d) Jika y adalah gas mulia, x adalah logam alkali.
Tabel periodik disusun dalam urutan menaik dari nomor atom.
Jika Y memiliki nomor atom z dan X memiliki satu proton lebih banyak dari itu, itu berarti bahwa kedua elemen ini berada dalam periode yang sama dan X setelah Y.
Contoh:
| Elemen | elemen selanjutnya |
| zkamu | z + 1X |
| 11Di | 12mg |
Kedua unsur tersebut berada pada periode ke-3 dan magnesium memiliki satu proton lebih banyak daripada natrium.
Menurut alasan ini kita harus:
a) SALAH. Logam alkali muncul sebelum logam alkali tanah pada tabel periodik. Pernyataan yang benar adalah: Jika y adalah logam alkali, x adalah alkali tanah.
b) SALAH. Sebuah halogen datang sebelum gas mulia pada tabel periodik. Pernyataan yang benar adalah: Jika y adalah halogen, x adalah gas mulia.
c) SALAH. Logam transisi dan gas mulia dipisahkan oleh unsur kimia lain dan karenanya tidak berurutan.
d) BENAR. Gas mulia adalah kelompok terakhir pada tabel periodik dan logam alkali yang pertama, jadi mereka berurutan.
Contoh:
| gas mulia | logam alkali |
| zkamu | z + 1X |
| 2dia | 3Baca |
Litium, logam alkali, memiliki satu proton lebih banyak daripada helium, yang merupakan gas mulia.
e) SALAH. X berada pada periode yang sama dengan Y tetapi setelahnya, tidak lebih awal dari keadaan alternatif.
pertanyaan 5
Dari nomor atom suatu unsur kimia dapat diketahui:
a) jumlah neutron dalam inti
b) jumlah elektron dalam elektrosfer
c) massa inti
Jawaban: b) jumlah elektron di elektrosfer
Sebuah atom dalam keadaan dasar netral secara listrik. Jadi, mengetahui nomor atom, yang sesuai dengan jumlah proton (partikel bermuatan positif), kita tahu jumlah elektron (partikel bermuatan negatif) di elektrosfer.
Misalnya, besi memiliki nomor atom 26, sehingga dalam keadaan dasar memiliki 26 elektron di sekitar inti.
Belajar lebih tentang unsur kimia ini adalah nomor atom.
Sifat periodik dan aperiodik
pertanyaan 1
(UFSM) Tentukan apakah pernyataan yang berkaitan dengan sifat periodik unsur benar (T) atau salah (F).
( ) Tergantung pada massa atom unsur-unsur.
( ) Mereka diulang pada interval yang kurang lebih teratur dalam kaitannya dengan peningkatan nomor atom.
( ) Sejenis dalam satu kelompok unsur.
( ) Sejenis dalam periode yang sama dari unsur-unsur.
( ) Dalam golongan yang sama, nilai numerik dari sifat periodik selalu meningkat ketika ada peningkatan nomor atom unsur.
Urutan yang benar adalah:
a) V - F - V - F - F
b) V - F - F - V - V
c) F - V - V - F - F
d) F - V - F - V - V
e) V - F - F - V - F
Alternatif yang benar: c) F - V - V - F - F
(SALAH) Tergantung pada massa atom unsur-unsur.
Menurut hukum periodisitas Moseley, banyak sifat fisik dan kimia dari unsur-unsur kimia bervariasi menurut nomor atom.
(BENAR) Mereka diulang pada interval yang kurang lebih teratur dalam kaitannya dengan peningkatan nomor atom.
Sifat-sifat seperti jari-jari atom, volume atom, massa jenis, titik leleh, dan titik didih adalah contoh sifat-sifat yang berulang secara teratur dalam tabel periodik.
(BENAR) Serupa dalam satu kelompok unsur.
Kelompok-kelompok tabel periodik telah diatur dengan unsur-unsur yang memiliki sifat serupa.
(SALAH) Sejenis dalam periode yang sama dari unsur-unsur.
Properti serupa dalam keluarga, bukan periode. Dalam periode, unsur-unsur didistribusikan dengan jumlah lapisan elektronik.
(SALAH) Dalam golongan yang sama, nilai numerik dari sifat periodik selalu meningkat ketika ada peningkatan nomor atom unsur.
Sifat dapat bertambah atau berkurang tergantung pada nomor atom. Contohnya adalah keelektronegatifan, yang berkurang dengan bertambahnya nomor atom dalam suatu golongan tertentu.
Baca juga: Sifat Periodik
pertanyaan 2
(FAESP) Sifat aperiodik dari unsur-unsur adalah:
a) massa jenis, volume atom, dan massa atom.
b) titik leleh, keelektronegatifan, dan kalor jenis.
c) volume atom, massa atom dan titik leleh.
d) massa atom, panas spesifik dan titik leleh.
e) massa atom dan panas spesifik.
Alternatif yang benar: e) massa atom dan kalor jenis.
Sifat aperiodik diulang secara berkala.
Massa atom adalah ukuran berat atom dalam satuan massa atom, yang sesuai dengan massa karbon-12.
Kalor jenis menentukan jumlah kalor yang dibutuhkan untuk menaikkan suhu sebesar 1 °C dari 1 g elemen.
Kedua sifat ini tidak berhubungan dengan posisi unsur pada tabel periodik.
Sifat-sifat lainnya diklasifikasikan sebagai periodik karena bertambah atau berkurang dengan nomor atom. Apakah mereka:
- Massa jenis: menyatakan hasil bagi antara massa dan volume suatu unsur.
- Volume atom: mewakili volume satu set atom dan mempengaruhi jarak di antara mereka.
- Titik lebur: suhu di mana transisi dari padat ke cair terjadi.
- Keelektronegatifan: kemampuan atom untuk menarik pasangan elektronik yang dimilikinya dalam ikatan kovalen.
Baca juga: keelektronegatifan dan Afinitas Elektronik
pertanyaan 3
(PUC-PR) Di antara diagram berikut yang berhubungan dengan tabel periodik, mana yang benar?
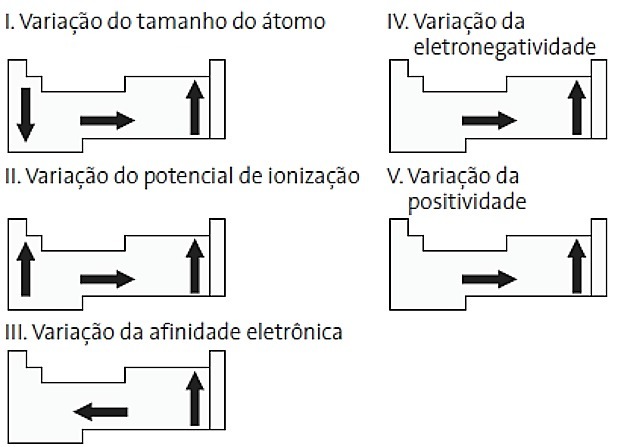
a) II dan V
b) II dan III
c) I dan V
d) II dan IV
e) III dan IV
Alternatif yang benar: d) II dan IV.
SAYA. SALAH. Variasi ukuran atom diukur dengan jarak rata-rata dari inti ke elektron terluar. Atom terbesar terletak di bagian bawah tabel, sehingga kenaikan terjadi sesuai dengan nomor atom dan representasi yang benar adalah:
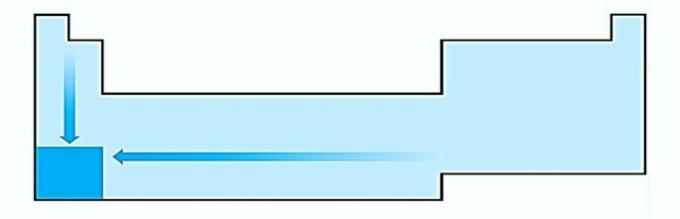
II. BENAR Energi yang diperlukan untuk melepaskan elektron dari atom yang terisolasi dalam keadaan gas disebut potensial ionisasi. Ini meningkat seperti yang ditunjukkan pada diagram pernyataan.
AKU AKU AKU. SALAH. Afinitas elektron menyatakan energi yang dilepaskan ketika atom netral dalam keadaan gas menerima elektron, menjadi sifat non-logam yang sangat penting. Afinitas elektronik tertinggi diamati pada halogen dan oksigen.
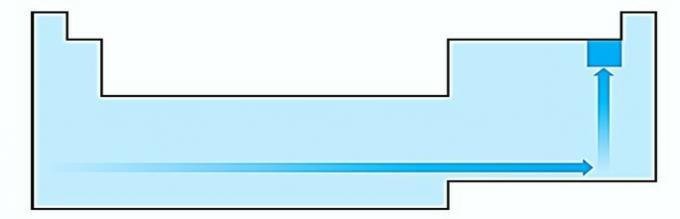
IV. BENAR Keelektronegatifan berhubungan dengan potensial ionisasi dan afinitas elektron. Dengan demikian, halogen adalah unsur yang paling elektronegatif pada tabel periodik.
V SALAH. Elektropositivitas terjadi dalam arah yang berlawanan dengan elektronegativitas. Ini mewakili kemampuan atom untuk melepaskan elektron.
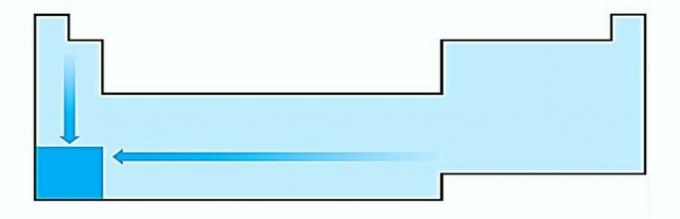
Oleh karena itu, logam alkali memiliki elektropositivitas tertinggi.
Terus uji pengetahuan Anda dengan daftar:
- Latihan tentang ikatan kimia
- Latihan tentang distribusi elektronik
- Latihan tentang model atom
- Latihan termokimia
