ITU Tabel periodik adalah model yang mengelompokkan semua unsur kimia yang diketahui dan sifat-sifatnya. Mereka disusun dalam urutan menaik nomor atom (jumlah proton).
Secara total, Tabel Periodik baru memiliki 118 unsur kimia (92 alami dan 26 buatan).
Setiap kotak menentukan nama unsur kimia, simbolnya, dan nomor atomnya.
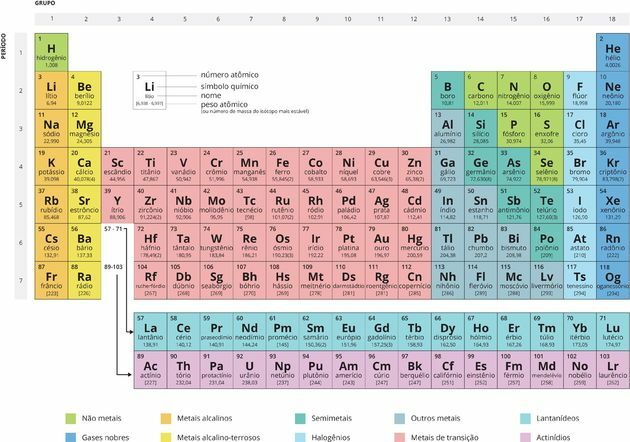
Organisasi Tabel Periodik
panggilan Periode mereka diberi nomor garis horizontal, yang memiliki elemen yang memiliki jumlah lapisan elektronik yang sama, berjumlah tujuh periode.
- periode pertama: 2 elemen
- periode ke-2: 8 elemen
- periode ke-3: 8 elemen
- Periode ke-4: 18 elemen
- Periode ke-5: 18 elemen
- Periode ke-6: 32 elemen
- Periode ke-7: 32 elemen
Dengan pengaturan periode dalam tabel, beberapa garis horizontal akan menjadi sangat panjang, sehingga deret lantanida dan deret aktinida biasanya dipisahkan dari yang lain.
Di Keluarga atau kelompok adalah kolom vertikal, di mana unsur-unsur memiliki jumlah elektron yang sama di kulit terluar, yaitu di in lapisan valensi. Banyak elemen dari kelompok-kelompok ini terkait menurut mereka sifat kimia.
Ada delapan belas Grup (A dan B), dan keluarga paling terkenal berasal dari Grup A, juga disebut elemen perwakilan:
- 1A Keluarga: Logam Alkali (litium, natrium, kalium, rubidium, sesium, dan fransium).
- Keluarga 2A: Logam Alkali-Bumi (beril, magnesium, kalsium, strontium, barium dan radium).
- Keluarga 3A: Keluarga boron (boron, aluminium, galium, indium, talium dan nihonium).
- Keluarga 4A: Keluarga karbon (karbon, silikon, germanium, timah, timbal dan flerovium).
- Keluarga 5A: Keluarga nitrogen (nitrogen, fosfor, arsenik, antimon, bismut dan muscovium).
- Keluarga 6A: Kalkogen (oksigen, belerang, selenium, telurium, polonium, livermorium).
- Keluarga 7A: halogen (fluor, klorin, brom, yodium, astatin, dan tenessin).
- Keluarga 8A: Gas mulia (Helium, Neon, Argon, Kripton, Xenon, Radon, dan Oganessonium).
Kamu elemen transisi, juga disebut logam transisi, mewakili 8 keluarga Grup B:
- keluarga 1B: tembaga, perak, emas dan rontgen.
- keluarga 2B: seng, kadmium, merkuri dan copernicus.
- Keluarga 3B: skandium, itrium dan serius lantanida (15 elemen) dan aktinida (15 elemen).
- Keluarga 4B: titanium, zirkonium, hafnium dan rutherfordium.
- keluarga 5B: vanadium, niobium, tantalum dan dubnium.
- Keluarga 6B: kromium, molibdenum, tungsten dan seaborgium.
- Keluarga 7B: mangan, teknesium, renium dan bohrium.
- keluarga 8B: besi, rutenium, osmium, hassium, kobalt, rhodium, iridium, meitnerium, nikel, paladium, platinum, darmstadium.
Dengan penetapan International Union of Pure and Applied Chemistry (IUPAC), kelompok-kelompok mulai diorganisir dengan angka dari 1 sampai 18, meskipun masih umum untuk menemukan keluarga digambarkan dengan huruf dan angka seperti yang ditunjukkan di atas.
Perbedaan penting yang dihasilkan oleh sistem baru yang disajikan oleh IUPAC adalah bahwa keluarga 8B sesuai dengan kelompok 8, 9 dan 10 dalam tabel periodik.
Tabel Periodik Hitam Putih
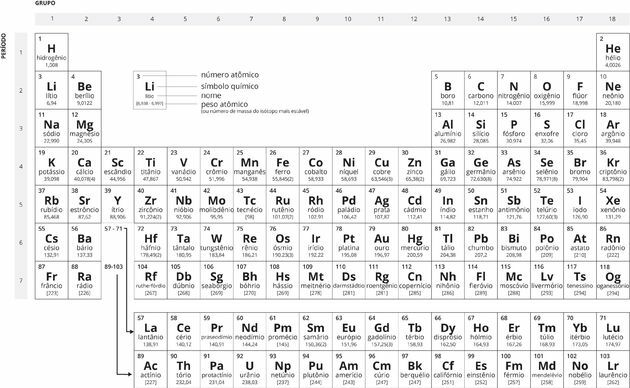
Sejarah Tabel Periodik
Tujuan mendasar membuat tabel adalah untuk memfasilitasi klasifikasi, organisasi, dan pengelompokan elemen sesuai dengan propertinya.
Sampai mencapai model saat ini, banyak ilmuwan membuat tabel yang dapat menunjukkan cara untuk mengatur unsur-unsur kimia.
Tabel Periodik paling lengkap dibuat oleh ahli kimia Rusia Dmitri Mendeleev (1834-1907), pada tahun 1869 karena massa atom dari elemen.
Mendeleev mengatur kelompok elemen menurut sifat yang sama dan meninggalkan ruang kosong untuk elemen yang dia yakini belum ditemukan.
Tabel Periodik seperti yang kita kenal sekarang ini disusun oleh Henry Moseley, pada tahun 1913, atas perintah nomor atom unsur kimia, reorganisasi tabel yang diusulkan oleh Mendeleev.
William Ramsay menemukan unsur-unsur neon, argon, kripton dan xenon. Unsur-unsur ini bersama dengan helium dan radon termasuk keluarga gas mulia dalam Tabel Periodik.
Glenn Seaborg menemukan unsur transuranik (nomor 94 sampai 102) dan pada tahun 1944 mengusulkan konfigurasi ulang Tabel Periodik, menempatkan rangkaian aktinida di bawah rangkaian lantanida.
Pada tahun 2019, tabel periodik berusia 150 tahun dan resolusi Perserikatan Bangsa-Bangsa dan UNESCO dibuat untuk menjadikan ini Tahun Tabel Periodik Internasional Unsur Kimia sebagai cara untuk mengenali salah satu ciptaan yang paling berpengaruh dan penting dari ilmu pengetahuan.
Keingintahuan Tabel Periodik
- Persatuan Internasional Kimia Murni dan Terapan Persatuan Internasional Kimia Murni dan Terapan - IUPAC) adalah sebuah LSM (Organisasi non-pemerintah) yang didedikasikan untuk studi dan kemajuan di Kimia. Di seluruh dunia, standar yang ditetapkan untuk Tabel Periodik direkomendasikan oleh Organisasi.
- 350 tahun yang lalu, unsur kimia pertama yang diisolasi di laboratorium adalah fosfor oleh alkemis Jerman Henning Brand.
- Unsur Plutonium ditemukan pada tahun 1940-an oleh ahli kimia Amerika Glenn Seaborg. Dia menemukan semua elemen transuranik dan memenangkan Hadiah Nobel pada tahun 1951. Elemen 106 dinamai Seaborgium untuk menghormatinya.
- Pada tahun 2016, elemen kimia baru dari tabel dibuat resmi: Tennessine (Ununséptio), Nihonium (Ununtrio), Moscovium (Ununpêntio) dan Oganesson (Ununóctio).
- Unsur-unsur kimia baru yang disintesis disebut super berat karena mengandung sejumlah besar proton, yang ternyata jauh lebih unggul daripada unsur-unsur kimia yang ditemukan di alam.
Ringkasan Tabel Periodik
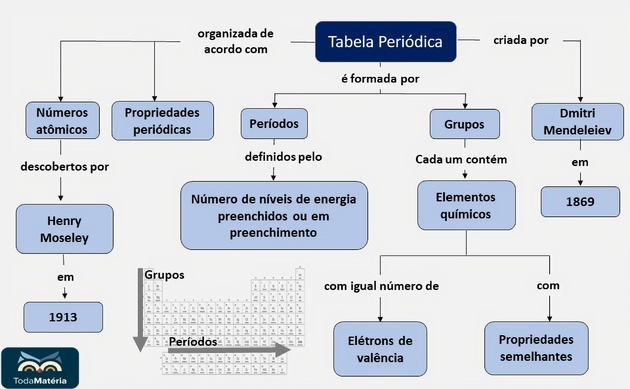
Periksa pertanyaan ujian masuk dengan resolusi komentar di Latihan pada Tabel Periodik dan pertanyaan yang tidak dipublikasikan di Latihan Pengorganisasian Tabel Periodik.