Hibridisasi karbon tipe sp2 itu terjadi ketika ia memiliki ikatan rangkap dan dua ikatan tunggal atau ikatan pi (π) dan ikatan tiga sigma (σ). Faktanya, hibridisasi sp2 itu terjadi antara atom-atom yang membentuk ikatan rangkap.
Contoh dari molekul tersebut adalah formaldehida (CH2HAI). Perhatikan strukturnya di bawah ini:
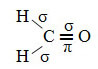
Seperti yang terlihat dalam teks "hibridisasi tipe sp3”, hibridisasi karbon terjadi ketika sebuah elektron dari sublevel 2s menerima energi dan “diangkut” ke 2p sublevel dan, dengan demikian, berasal dari 4 orbital hibridisasi dari "campuran" orbital atom murni.
Dalam kasus formaldehida, kita tahu bahwa akan ada ikatan pi, jadi salah satu orbital hibridisasi ini dicadangkan untuk ikatan ini, sedangkan tiga lainnya membawa ikatan sigma:
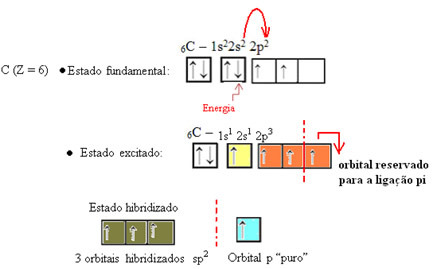
Atom hidrogen yang membuat ikatan tunggal dengan karbon, membuatnya dengan orbital s-nya:
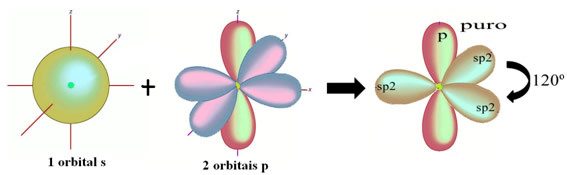
Orbital p "murni" yang tersisa mengikat ganda atom oksigen dan molekul formaldehida memiliki struktur berikut:
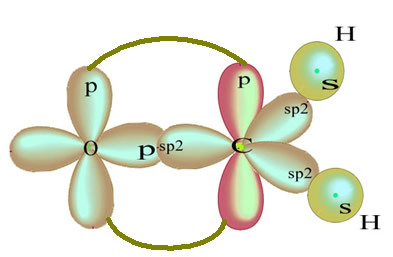
Adapun jenis ikatan yang ada dalam struktur formaldehida ini, kami memiliki:

Koneksi: 1 = 2 = σs-sp2
3 = σp-sp2
4 =πp-p
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp2.htm
