Di reaksi eliminasi organik adalah mereka di mana atom atau kelompok atom dari suatu molekul dihilangkan atau dihilangkan darinya, menciptakan senyawa organik baru, selain senyawa anorganik yang dibentuk oleh bagian yang dihapus.
Salah satu jenis reaksi eliminasi adalah dehidrasi, di mana molekul yang hilang adalah air. Dehidrasi alkohol (senyawa yang memiliki gugus OH yang terikat pada karbon jenuh dalam rantai terbuka) dapat terjadi dengan dua cara: intramolekul dan antarmolekul.
"Intra" berarti "di dalam", oleh karena itu, dehidrasi intramolekul alkohol terjadi ketika molekul air keluar dari "dalam" molekul alkohol itu sendiri. Dalam hal ini, produk organik yang terbentuk akan menjadi alkena.
Reaksi ini terjadi hanya dengan adanya katalis yang bertindak sebagai pengering, dan sebagian besar waktu itu adalah asam sulfat pekat (H2HANYA4) dan suhu harus sekitar 170ºC.
Contoh:
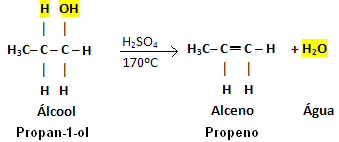
Perhatikan bahwa gugus OH pergi dan hidrogen meninggalkan karbon tetangga, sehingga menimbulkan air. Selanjutnya, ikatan rangkap yang memunculkan alkena dibuat.
Fasilitas untuk mengalami dehidrasi mengikuti urutan sebagai berikut:
Alkohol tersier > Alkohol sekunder > Alkohol primer
Tapi bagaimana ketika gugus OH berada di tengah rantai karbon? Atom hidrogen dari mana atom karbon tetangga akan dilepaskan dan membentuk molekul air?
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
Misalnya, berikutnya adalah 2-metilpentan-3-ol. Perhatikan bahwa satu atom karbon tetangga adalah tersier (disorot dengan warna merah), sedangkan yang lainnya adalah sekunder (disorot dengan warna biru):
H OH H
│ │ │
H3C Ç ─ Ç ─ Ç CH3
│ │ │
H H CH3
Hidrogen yang terikat pada atom karbon tersier akan lebih mudah lepas, karena sifat elektronegatifnya sama dengan+1Dengan demikian, semakin kecil karakter negatif karbon, semakin lemah ikatan di antara mereka dan semakin mudah untuk memutuskan ikatan mereka.
Dalam kasus seperti ini, semua senyawa yang mungkin terbentuk, namun, dominasi akan diberikan dalam urutan: Alkohol tersier > Alkohol sekunder > Alkohol primer.
Jadi kita punya:
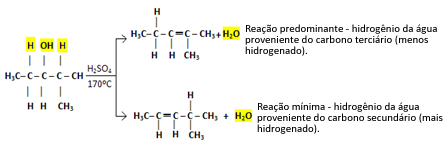
Jenis reaksi ini mematuhi Aturan Saytzef, yang mengatakan bahwa akan ada kecenderungan lebih besar bagi hidrogen untuk meninggalkan karbon lebih sedikit terhidrogenasi. Aturan ini persis kebalikan dari Aturan Markovnikov digunakan untuk reaksi adisi.
Untuk melengkapi pengetahuan Anda tentang hal ini, baca juga teks "Dehidrasi Antarmolekul Alkohol”.
Oleh Jennifer Fogaa
Lulus kimia
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
FOGAÇA, Jennifer Rocha Vargas. "Dehidrasi Alkohol Intramolekuler"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/quimica/desidratacao-intramolecular-dos-Alcoois.htm. Diakses pada 28 Juni 2021.


