Dalam teks "isomer geometri atau cis-trans” ditunjukkan bagaimana isomerisme spasial geometris atau cis-trans. Secara singkat, isomer cis sesuai dengan senyawa yang ligan yang sama pada setiap atom karbon berada di bidang yang sama; sudah di isomer trans, mereka berada di sisi yang berlawanan.
Ini diidentifikasi oleh asal usul istilah ini, yang berasal dari bahasa Latin, di mana cis berarti "di sebelah" dan trans "seberang".
Nomenklatur ini sangat berguna ketika dua karbon masing-masing hanya memiliki dua ligan yang berbeda. Namun, istilah-istilah ini dapat menjadi ambigu ketika mengacu pada alkena, yang atom karbon ikatan rangkapnya memiliki lebih dari dua ligan berbeda dalam himpunan.
Sebagai contoh, perhatikan senyawa di bawah ini:

Perhatikan bahwa pada karbon x ligan nomor atom terendah adalah CH3, dan pada karbon kamu adalah H Tetapi jika kita menempatkan bahwa senyawa ini adalah isomer cis, pertanyaan berikut dapat muncul: seperti apa dia? cis jika gugus penghubungnya sama (CH3) berada di sisi yang berlawanan?
Oleh karena itu, untuk menghindari ambiguitas ini, dalam kasus ini lebih tepat menggunakan nomenklatur E-Z, di mana huruf E berasal dari kata Jerman. entgegen, yang berarti "berlawanan" dan Z berasal dari kata Jerman zusammen, yang berarti “bersama”. Nomenklatur ini mengikuti aturan berikut:

Menerapkan aturan prioritas ini ke 2-chlorobu-2-ene, kami memilikinya di karbon x ligan dengan nomor atom tertinggi adalah Cl, dan pada karbon kamu adalah CH3. Dengan demikian, kami memiliki isomer berikut:
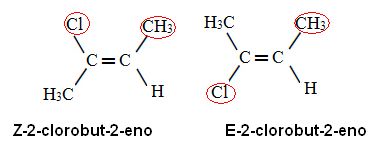
Dalam kasus pertama, ligan dengan nomor atom tertinggi berada di sisi bidang yang sama (Z) dan yang kedua, mereka berada di sisi yang berlawanan (E).
Ini juga terjadi dengan senyawa siklik. Penting untuk diingat bahwa tidak benar menghubungkan istilah cis dan Z, dan trans dan E, karena keduanya adalah sistem penamaan yang berbeda.
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/isomeria-e-z-no-lugar-cis-trans.htm
