Kamu Hidrokarbon tersusun dibentuk oleh karbon (C) dan hidrogen (H). Fleksibilitas karbon, yang merupakan elemen utama dari senyawa ini, mendukung keberadaan struktur yang sangat beragam Oleh karena itu, beberapa sifat, seperti titik leleh dan titik didih, mungkin berbeda antara satu hidrokarbon dengan hidrokarbon lainnya.
Mereka sebagian besar adalah molekul apolar, dengan kekuatans antarmolekul jenis dipol terinduksi dan kepadatan kurang dari Itu dari air. Identifikasi senyawa tersebut dapat dilakukan melalui tata nama yang mengikuti aturan yang ditetapkan oleh International Union of Pure and Applied Chemistry (Iupac).
Baca juga: Karbon - salah satu unsur paling melimpah di Alam Semesta
Sifat-sifat hidrokarbon

Polaritas: hidrokarbon tanpa adanya heteroatom adalah apolar.
Gaya antarmolekul: ikatan antara molekul-molekul hidrokarbon adalah jenis dipol yang diinduksi.
titik leleh dan danmendidih: bervariasi sesuai dengan ukuran, fungsi dan organisasi struktural molekul.
keadaan fisik: di bawah kondisi suhu dan tekanan normal, hidrokarbon dengan empat atau lebih sedikit atom karbon berada dalam keadaan gas. Mereka dengan 5 hingga 17 karbon berada dalam keadaan cair, dan hidrokarbon dengan lebih dari 17 karbon adalah zat padat.
Massa jenis: lebih kecil dari massa jenis air, yaitu kurang dari 1,0 g/cm³.
Reaktivitas: hidrokarbon alifatik dan tak jenuh kurang reaktif; senyawa tak jenuh lebih cenderung bereaksi dengan molekul lain, dan hidrokarbon siklik dengan hingga lima karbon sangat reaktif.
Klasifikasi hidrokarbon
Hidrokarbon dapat diklasifikasikan oleh organisasi struktural rantai dan oleh instansi.ketidakjenuhan adalah adanya ikatan rangkap dua atau rangkap tiga antara karbon, adalah terjadinya koneksi tipe pi (π). sudah ranting mereka seperti "cabang" yang melekat pada struktur hidrokarbon yang lebih besar. Rantai siklik juga dapat mengandung cabang dan/atau ketidakjenuhan – organisasi struktural hidrokarbon rantai tertutup membentuk poligon seperti persegi, segitiga, heksana, dan lain-lain.
Mengenai susunan atom, hidrokarbon dapat memiliki rantai normal atau bercabang.
→ C hidrokarbongaris normal, linier atau lurus straight: yang memiliki tali yang hanya memiliki dua ujung.

→ C hidrokarbonmembenci bercabang: satu dengan rantai yang memiliki lebih dari dua ujung. Untuk mengetahui di mana dan apa cabangnya, penting untuk memilih rantai utama dengan benar. Rantai utama harus mengandung semua ketidakjenuhan dan heteroatom (jika ada), sebaik jumlah terbesar dari karbon berurutan. Karbon yang tidak terdapat pada rantai utama adalah cabang.
Contoh:

Sehubungan dengan "penutupannya", hidrokarbon dapat memiliki rantai tertutup, terbuka atau campuran.
→ Rantai hidrokarbons tertutup atau siklik: mereka dengan rantai di mana atom mengatur diri mereka sendiri membentuk siklus, poligon atau cincin aromatik (hidrokarbon tertutup dengan ketidakjenuhan bergantian). Jangan memiliki ujung yang longgar kecuali ada cabang. Setiap titik poligon mewakili karbon dan agen ikatan hidrogen masing-masing.
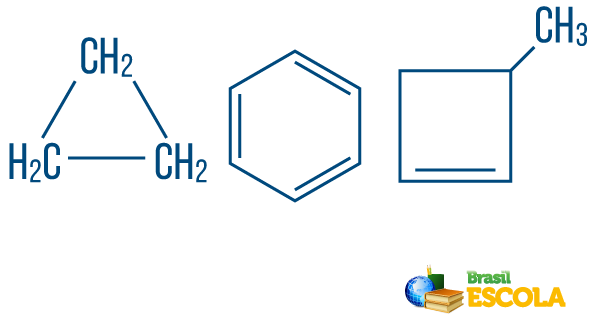
→ Hidrokarbon rantai terbuka atau asiklik: adalah mereka dengan rantai yang memiliki setidaknya dua ujung.

→ Hidrokarbon dari string tipe campuran: dibentuk oleh cincin atau rantai siklik yang melekat pada bagian linier; memiliki setidaknya satu ujung.
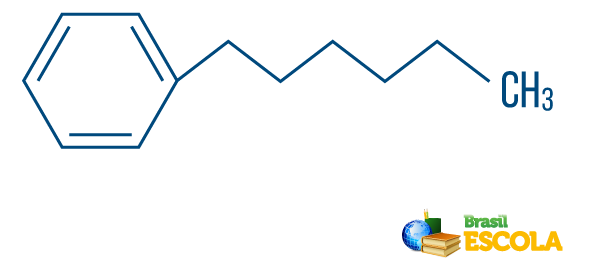
Baca juga: Hidrokarbon aromatik - contoh dan sifat
Tata nama hidrokarbon
Untuk setiap jenis hidrokarbon, ada aturan penamaan yang ditetapkan oleh Iupac. Tata nama senyawa ini dilakukan sebagai berikut:
bagian pertama: lokasi dan nama cabang (jika ada);
bagian ke-2: istilah itu berlaku siklus jika senyawa itu adalah rantai tertutup, tetapi jika itu adalah rantai alifatik (terbuka), itu tidak perlu;
bagian ke-3: awalan yang menunjukkan berapa banyak karbon yang ada di rantai utama;
bagian ke-4: lokasi dan infiks yang menunjukkan jenis ketidakjenuhan dalam molekul;
bagian ke-5: akhiran "o" yang tepat untuk hidrokarbon.
Jika molekul memiliki struktur terbuka, tanpa percabangan, tata nama akan dimulai pada bagian 3.
Tabel berikut menunjukkan informasi yang diperlukan (awalan, sisipan, dan akhiran) untuk tata nama hidrokarbon secara umum. HAI awalan bervariasi dengan jumlah karbon; HAI infiks, sesuai dengan jumlah ketidakjenuhan; ini adalah akhiran“HAI" mengacu pada senyawa jenis hidrokarbon.
Awalan |
Infiks |
Akhiran |
||
1 karbon |
bertemu- |
Hanya panggilan tunggal |
-sebuah- |
-HAI |
2 karbon |
et- |
|||
3 karbon |
menopang- |
1 ikatan rangkap |
-en- |
|
4 karbon |
tapi- |
|||
5 karbon |
terpendam- |
2 ikatan rangkap |
-dien- |
|
6 karbon |
hex- |
|||
7 karbon |
hept- |
1 ikatan rangkap tiga |
-di- |
|
8 karbon |
okt- |
|||
9 karbon |
non- |
2 tautan rangkap tiga |
-diin- |
|
10 karbon |
dek- |
Langkah pertama dalam menemukan nomenklatur senyawa organik adalah mengidentifikasi rantai utama karbon, yang harus mengandung ketidakjenuhan dan sebanyak mungkin karbon berurutan. Setelah mengidentifikasi rantai utama, karbon harus disebutkan – mulai menghitung dari sisi yang paling dekat dengan cabang dan ketidakjenuhan (jika ada). ITU lokalisasi akan menjadi jumlah karbon di mana cabang atau ketidakjenuhan ditemukan. Kadang-kadang hanya ada satu kemungkinan lokasi untuk ikatan radikal atau rangkap dua atau rangkap tiga, sehingga tidak perlu menyatakan lokasi karbon penghubung dalam tata nama.

ITU nomenklatur untuk cabang akan diberikan oleh jumlah karbon di masing-masing, ditambah terminasi garis atau ll. Ketika ada lebih dari satu cabang, urutan abjad digunakan.
Lihat contoh di bawah ini:
→ Contoh 1
CH3 – CH2 – CH3 → propana
Bagian pertama: awalan “menopang-” menunjukkan rantai memiliki tiga karbon.
bagian 2: sisipan "-sebuah-” menandakan bahwa molekul hanya membuat koneksi jenis sigma atau sederhana.
Bagian 3: akhiran "-HAI” adalah karakteristik dari hidrokarbon.
→ Contoh 2
CH2=CH-CH2-CH3 → Tapi-1-ena
Dalam hidrokarbon dengan ketidakjenuhan, perlu untuk nomor dan menemukan karbon di mana pasangan ditemukan, dan penomoran harus sekecil mungkin. Untuk ini, penghitungan karbon harus dimulai dengan sisi yang paling dekat dengan ikatan rangkap.
bagian pertama: "tapi-" menunjukkan bahwa ada empat karbon dalam rantai.
bagian ke-2: "1-en" mengacu pada ketidakjenuhan yang terletak antara karbon 1 dan 2.
bagian ke-3: "-HAI" adalah akhiran karakteristik hidrokarbon.
→ Contoh 3

bagian 1: "3-etil" menandakan bahwa ada cabang dua karbon pada karbon 2.
bagian ke-2: "-terpendam-" menunjukkan adanya lima karbon dalam rantai utama.
bagian ke-3: "-sebuah-" adalah infiks yang diterapkan pada rantai tak jenuh (tidak ada ikatan rangkap atau rangkap tiga).
bagian ke-4: "-HAI" adalah akhiran karakteristik hidrokarbon.
→ Contoh 4
Untuk rantai dengan lebih dari satu cabang, tempatkan radikal dalam nomenklatur dalam urutan abjad. Jika ada cabang dan ketidakjenuhan dalam molekul yang sama, penghitungan karbon dalam rantai utama harus dilakukan sedemikian rupa sehingga jumlah angka lokasi sekecil mungkin.
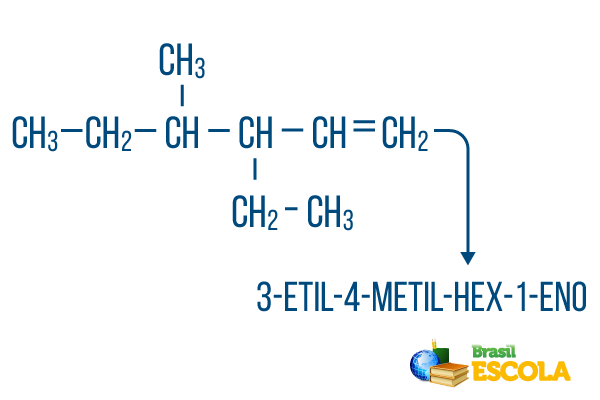
Penghitungan karbon rantai utama dilakukan dari kiri ke kanan, dan jumlah dari bilangan tak jenuh dan lokasi cabang adalah: 1+4+3 = 8. Jika penghitungan karbon dari kanan ke kiri, tata nama senyawanya adalah 4-etil-3-metil-5-ena, yang jumlah lokasinya adalah: 4+3+5 = 12, yang lebih besar dari hipotesis lainnya, sehingga tidak boleh digunakan.
bagian 1: 3-etil-4-metil membuat referensi ke radikal dalam urutan abjad dan lokasi masing-masing.
bagian ke-2: hex- berarti ada 6 karbon dalam rantai utama.
bagian ke-3: 1-en menunjukkan adanya ikatan rangkap pada karbon 1.
bagian ke-4: "-HAI" adalah akhiran karakteristik hidrokarbon.
→ Contoh 5
Untuk string tertutup, aturan penamaan berlaku, tetapi kata siklus memulai nama senyawa, menunjukkan bahwa itu adalah hidrokarbon tertutup atau siklik.
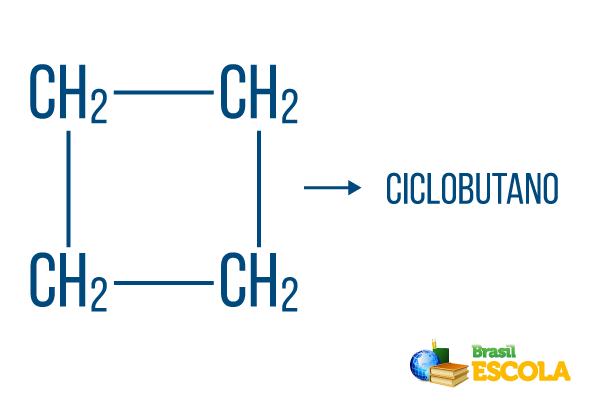
bagian 1: siklus- menunjukkan bahwa itu adalah string tertutup.
bagian ke-2: -tapi- menunjukkan adanya 4 karbon dalam rantai
bagian ke-3: -HAIadalah akhiran karakteristik hidrokarbon.
Baca juga: Klasifikasi rantai karbon
Jenis-jenis Hidrokarbon
Hidrokarbon dapat dibagi menjadi alkana, alkena, alkuna dan alkadiena - yang diklasifikasikan sebagai sesuai dengan pembentukan rantai (ikatan ganda atau rangkap tiga) - dan cyclans, yang merupakan rantai Tutup.
→ Alkana: adalah hidrokarbon yang tidak memiliki ketidakjenuhan. Rumus umum alkana adalah CtidakH2n+2, dan tidakpertanda itu disusun oleh awalan + sebuah + HAI.
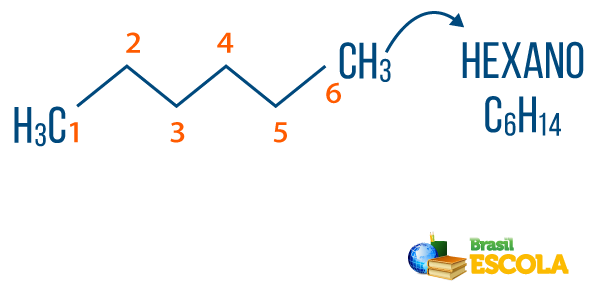
Kamu alkana dapat ditemukan di alam, seperti gas metana (CH4), yang dilepaskan oleh hewan dan diproduksi dalam proses dekomposisi, serta di kilang dan industri petrokimia. Senyawa seperti propana (Ç3H7), butana (Ç4H10), yang membentuk gas memasak (LPG) kami, dan oktan (Ç8H18), hadir dalam bahan bakar otomotif, adalah produk sampingan dari Minyak bumi.

→ alkena atau alkena: adalah rantai karbon yang memiliki ikatan rangkap tidak jenuh. Rumus umumnya adalah CtidakH2n, dan punya anda tidakpertanda itu disusun oleh Pmemperbaiki + id + o.

HAI gas etilen (Ç2H4), digunakan dalam pertanian untuk mempercepat pematangan buah-buahan, termasuk fungsi alkena. Senyawa ini juga digunakan dalam produksi bahan baku polietilena, digunakan dalam pembuatan peralatan plastik.
→ Alkuna atau asetilena: Hidrokarbon dengan ikatan rangkap tiga. Rumus umumnya adalah CtidakH2n - 2. ITU tata nama itu disusun oleh awalan + di + o.

HAI asetilen atau etin (C2H2) adalah gas dari fungsi alkuna yang digunakan dalam las dan pemotongan logam metal. Senyawa ini dapat mencapai suhu hingga 3.000 °C, yang memungkinkan perbaikan dilakukan pada bagian kapal yang terendam.

→ alkadiena atau diena: rantai karbon dengan dua ketidakjenuhan, yaitu, dua ikatan rangkap antara karbon. Rumus umum untuk fungsi ini adalah C.tidakH2n - 2. Sadarilah bahwa itu rumus yang sama dengan alkuna, yang berarti itu bisa terjadi isomerisme antar senyawa (rumus molekul yang sama untuk senyawa yang berbeda).
Tata nama suatu alkana terdiri dari: Pmemperbaiki + dien + o.
Contoh:

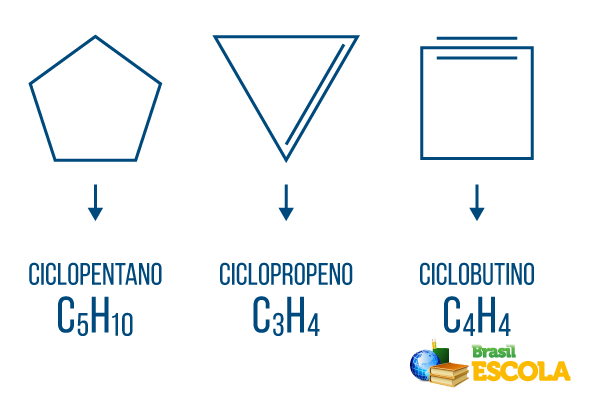
→ Hidrokarbon rantai tertutup: molekul-molekul mengatur diri mereka sendiri dengan cara siklik, cenderung membentuk poligon dan, seperti dalam rantai terbuka, mungkin ada pembentukan dan/atau percabangan. Siklon, siklus, siklin, dan benzena adalah hidrokarbon rantai tertutup.
Siklon atau sikloalkana: rantai siklik yang hanya terdiri dari ikatan tunggal. Rumus umumnya adalah CtidakH2n. Nomenklatur: ciclo + awalan + an + o.
Siklus atau sikloalkena: rantai hidrokarbon tertutup dengan pembentukan. Rumus umumnya adalah CtidakH2n-2. Tata nama: çiclo + awalan + en + HAI.
-
Siklin atau sikloalkuna: hidrokarbon rantai tertutup dengan adanya dua ikatan rangkap. Rumus umumnya adalah CtidakH2n-4. Tata nama: çiclo + awalan + di + o.
benzena
Benzena adalah jenis hidrokarbon rantai tertutup dengan enam karbon di mana ikatan bervariasi antara tunggal dan ganda. Senyawa-senyawa tersebut adalah racun dan sangat karsinogenik, digunakan sebagai pelarut organik dalam proses kimia.
Agar hidrokarbon dianggap aromatik, setidaknya harus ada satu cincin benzena, yang sangat reaktif, oleh karena itu tunduk pada dua atau lebih pengganti, yang akan kita lihat di sini sebagai konsekuensi. Ketika ada dua radikal penghubung, kita akan memiliki nama khusus untuk setiap pasangan posisi.
Radial pada 1,2 karbon benzena → orto
Radikal pada 1,3 karbon benzena → tujuan
Radial pada karbon1,4 dari benzena → untuk
Annomenklatur senyawa aromatik dilakukan sebagai berikut:
Bagian 1: penempatan ligan (orto, tujuan atau to).
Bagian 2: nama radikal atau radikal yang terikat pada benzena (metil, etil, propil…). Nama yang diberikan untuk radikal mengikuti aturan hidrokarbon lainnya.
- bagian ke-3: -Bmeracuni, yang merupakan istilah karakteristik dari hidrokarbon aromatik.
Contoh:
→ Orto-dimetil-benzena

bagian 1: HAIrto- menunjukkan bahwa radikal diposisikan pada karbon 1 dan 2.
bagian ke-2: -dimetil- mengacu pada dua radikal, keduanya dengan satu karbon.
Bagian 3: -benzena adalah istilah karakteristik untuk hidrokarbon aromatik.
→ Orto-etil-metil-benzena
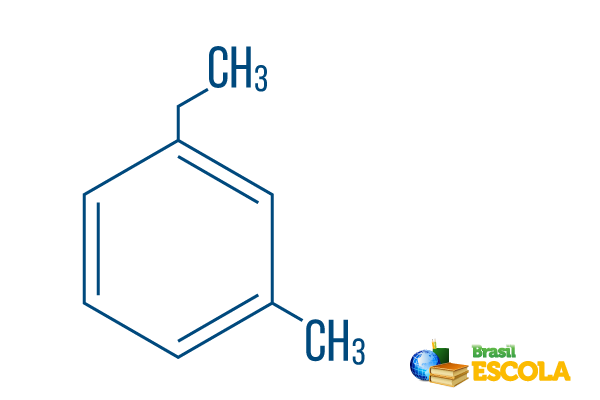
bagian 1: sayaoh- menunjukkan bahwa radikal diposisikan pada karbon 1 dan 3.
bagian ke-2: etil-metil- mengacu pada jumlah karbon di setiap radikal, karena etil Itu cabang dua karbon dan metil bercabang dengan satu karbon – ditempatkan dalam nomenklatur dalam urutan abjad.
Bagian 3: -benzena adalah istilah karakteristik untuk hidrokarbon aromatik.
→ para-dietil-benzena
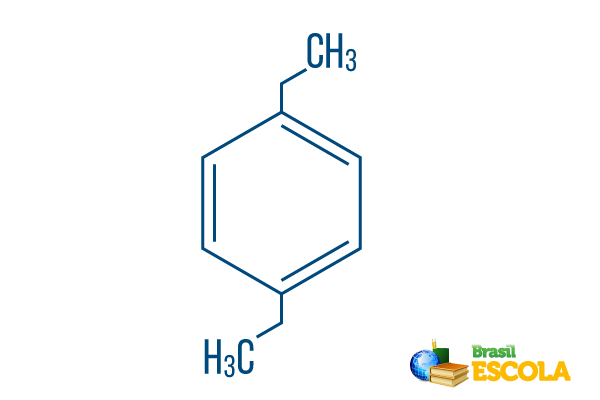
bagian 1: Pbajak- menunjukkan bahwa radikal berada pada karbon 1 dan 4 dari benzena.
bagian ke-2: -dietil- membuat referensi ke dua radikal dari tipe etil, yaitu, dua cabang dengan masing-masing dua karbon.
Bagian 3: -benzena adalah istilah karakteristik untuk hidrokarbon aromatik.
Baca juga:Penemuan struktur benzena
latihan yang diselesaikan
(Unsp) – Oktan adalah salah satu penyusun utama bensin, yang merupakan campuran dari hidrokarbon. Rumus molekul oktan adalah:
a) C8H18
b) C8H16
c) C8H14
d) C12H24
e) C18H38
Jawaban: huruf a). Menganalisis nomenklatur senyawa oktan, itu adalah alkana, yaitu molekul yang hanya terdiri dari ikatan tunggal. Jika rumus umum alkana adalah CtidakH2n+2, menggantikan “n” dengan delapan, yang merupakan jumlah karbon dalam rantai utama – dan unik dalam hal ini –, kita akan mendapatkan bahwa rumus molekul oktan adalah C8H18.
(UFSCar-SP) – Perhatikan pernyataan berikut tentang hidrokarbon.
I) Hidrokarbon adalah senyawa organik yang hanya terdiri dari karbon dan hidrogen.
II) Hanya hidrokarbon tak jenuh rantai lurus yang disebut alkena.
III) Sikloalkana adalah hidrokarbon alifatik jenuh dengan rumus umum CnH2n.
IV) Adalah hidrokarbon aromatik: bromobenzena, p-nitrotoluena dan naftalena.
Pernyataan berikut ini benar:
a) I dan III saja.
b) I, III dan IV saja.
c) II dan III saja.
d) III dan IV saja.
e) I, II dan IV saja.
Jawaban: Huruf a).
II - Alkena adalah senyawa dengan ikatan rangkap, yaitu tak jenuh, tetapi mereka dapat memiliki percabangan dalam rantainya, tidak secara eksklusif linier.
IV - Senyawa brometobenzena dan p-nitrotoluena milik lainnya fungsi organik.
oleh Laysa Bernardes
guru kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/hidrocarbonetos.htm
