Gas dan Uap
Perbedaan antara gas dan uap diberikan dari suhu kritis. Uap adalah materi dalam keadaan gas, keadaan yang dapat dicairkan dengan meningkatnya tekanan. Gasnya tidak sama. Ini adalah cairan yang tidak dapat dicairkan dengan peningkatan tekanan sederhana. Ini membuat gas berbeda dari uap.
Perilaku Gas
Suatu zat tertentu dalam keadaan gas adalah gas jika suhunya lebih tinggi dari suhu kritis, jika suhunya sama dengan atau lebih rendah dari suhu kritis zat tersebut adalah uap.
Gas-gas nyata yang biasa kita kenal, seperti helium, nitrogen dan oksigen, memiliki karakteristik molekul yang berbeda dan khusus masing-masing. Namun, jika kita menempatkan semuanya pada suhu tinggi dan tekanan rendah, mereka mulai menunjukkan perilaku yang sangat mirip. Dalam mempelajari gas, model teoretis sederhana diadopsi, yang dalam praktiknya tidak ada, dengan perilaku yang mirip dengan gas nyata. Perkiraan ini menjadi lebih baik semakin rendah tekanan dan semakin tinggi suhu. Model gas ini disebut gas sempurna
Sekitar abad 17 dan 19, tiga ilmuwan (Jacques Charles, Louis J. Gay-Lussac dan Paul E. Clayperon), setelah mempelajari perilaku gas, menguraikan hukum yang mengatur perilaku gas sempurna, juga disebut gas ideal. Hukum yang ditentukan oleh mereka menetapkan aturan perilaku "eksternal" dari gas sempurna, yang mengarah ke hanya menghitung besaran fisis yang berhubungan dengannya, yaitu: volume, suhu dan tekanan.
Hukum umum gas sempurna
Ekspresi yang menentukan hukum umum untuk gas sempurna dapat dilihat sebagai berikut:
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
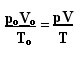
dimana pHAI, VHAI dan THAI adalah tekanan awal, volume awal dan suhu awal, masing-masing. Ini adalah ekspresi yang digunakan ketika variabel gas bervariasi.
Hukum Boyle
Robert Boyle, fisikawan dan kimiawan, adalah orang yang menentukan hukum yang mengatur transformasi yang dialami oleh gas, ketika suhunya dijaga konstan. Hukumnya mengatakan bahwa ketika gas mengalami transformasi isotermal, tekanannya berbanding terbalik dengan volume yang ditempati. Dari hukum ini kita peroleh bahwa bagaimana THAI = T Kita harus:
PHAIVHAI = pV
hukum Charles
Hukum Charles adalah hukum yang mengatur transformasi gas sempurna menjadi volume konstan. Transformasi ini disebut transformasi isokhorik atau isometrik. Menurut hukum ini, ketika massa gas sempurna mengalami transformasi isokhorik, tekanannya berbanding lurus dengan suhu absolutnya. Secara matematis hukum ini dapat dinyatakan sebagai berikut:

dimana pHAI dan THAI adalah tekanan awal dan suhu awal masing-masing.
Hukum Gay-Lussac
Hukum Gay-Lussac adalah hukum yang mengatur transformasi gas sempurna pada tekanan konstan. Hukum ini, meskipun menyandang nama Gay-Lussac, telah ditemukan oleh fisikawan dan kimiawan A.C. Charles. Menurut hukum, ketika gas mengalami transformasi isobarik, volume gas berbanding lurus dengan suhu mutlaknya. Secara matematis hukum ini dapat dinyatakan sebagai berikut:

Dimana VHAI dan THAI sesuai masing-masing dengan volume awal dan suhu awal.
Oleh Marco Aurélio da Silva
Lihat lebih banyak!!
Transformasi Gas
Mengetahui apa itu transformasi gas.
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
SANTOS, Marco Aurélio da Silva. "Studi Gas"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/fisica/estudo-dos-gases.htm. Diakses pada 27 Juni 2021.