HAI perhitungan massa atom dari suatu unsur adalah sumber matematika yang digunakan untuk menentukan nilai massa yang ada dalam Tabel Periodik dari masing-masing unsur kimia yang ada. Pada umumnya untuk melaksanakan perhitungan massa atom, kita harus mengetahui variabel berikut dari unsur kimia:
isotop elemen;
Nomor massa masing-masing isotop unsur;
Persentase masing-masing isotop unsur di alam.
Perhitungan massa atom Hidrogen, misalnya, dilakukan berdasarkan data berikut:
Menampilkan isotop protium (H1), deuterium (H2) dan tritium (H3);
Massa isotop ini masing-masing adalah 1, 2 dan 3;
Persentase Protium di alam adalah 98,9%;
Persentase Deuterium di alam adalah 0,09%;
Persentase Tritium di alam adalah 0,01%.
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
Standar matematika untuk menghitung massa atom
Untuk melaksanakan perhitungan massa atom dari setiap unsur kimia, kita harus menggunakan pola matematika berikut:
1HAI: kalikan nomor massa masing-masing isotop dengan persentasenya;
2HAI: tambahkan semua hasil yang ditemukan pada perkalian langkah pertama;
3HAI: bagi jumlah yang ditemukan dengan 100.
MA = nomor massa.persentase + nomor massa.persentase
100
Peta Pikiran: Massa Atom
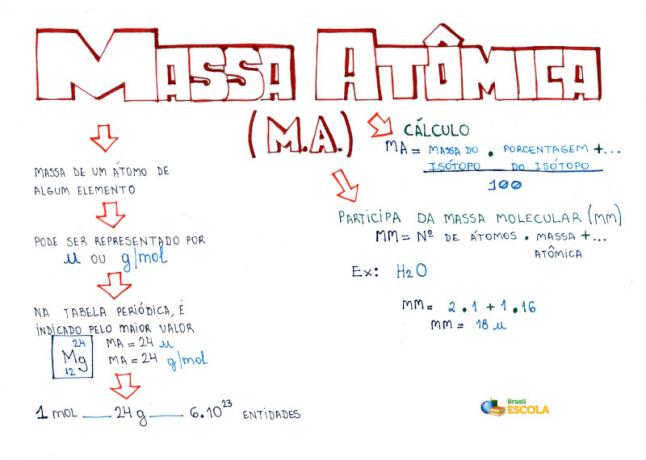
*Untuk mengunduh peta pikiran dalam PDF, Klik disini!
Contoh Perhitungan Massa Atom
Contoh pertama: Perhitungan massa atom Sulfur.
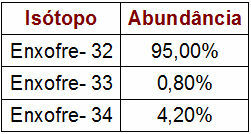
Persentase dan Data Massa Isotop Sulfur
Tabel yang disediakan menunjukkan nomor massa dan persentase masing-masing isotop belerang di alam. Untuk melakukan perhitungan massa atom, cukup lakukan langkah-langkah berikut:
1HAI Langkah: kalikan nomor massa masing-masing isotop dengan nilai kelimpahannya.
Belerang - 32 (S32)
s32 = 32.95
s32 = 3040
Belerang - 33 (S33)
s33 = 33.0,8
s33 = 26,4
Belerang - 34 (S34)
s34 = 34.4,2
s34 = 142,8
2HAI Langkah: tambahkan nilai yang ditemukan dalam perkalian nomor massa dan kelimpahan isotop.
Jumlah = S32 + S33 + S34
Jumlah = 3040 + 26,4 + 142,8
Jumlah = 3209,2
3HAI Langkah: hitung massa atom dengan membagi jumlah hasil yang ditemukan dengan 100:
MA = Jumlah
100
MA = 3209,2
100
MA = 32.092 u
Contoh ke-2: Unsur kimia tertentu (D) memiliki tiga isotop, yang nomor massanya adalah:
30D 32D 34D
Mengetahui bahwa massa atom unsur ini adalah 32,20 u dan ada 20% dari isotop 32D di alam, berapakah nilai persentase isotop lainnya?
Pernyataan tersebut memberikan nomor massa, massa atom dan persentase salah satu isotop. Untuk menentukan persentase isotop lain, kita harus melakukan langkah-langkah berikut:
1HAI Langkah: tentukan persentase masing-masing isotop.
Isotop - 30 (DS30)
DS30 = 30.x
DS30 = 30x
Isotop - 32 (DS32)
DS32 = 32.20
DS32 = 640
Isotop - 34 (D34)
DS34 = 34.y
DS34 = 34 tahun
2HAI Langkah: menggunakan semua data yang ditemukan dalam ekspresi matematika untuk menghitung massa atom.
MA = nomor massa.persentase + nomor massa.persentase
100
32,2 = 30x + 640 + 34th
100
32,2.100 = 30x + 640 + 34th
100
3220 - 640 = 30x+34y
30x + 34y = 2580
x = 2580 - 34 tahun
30
3HAI Langkah: gunakan ekspresi yang ditemukan di atas dari alasan berikut:
Persentase Isotop 1 + Persentase Isotop 2 + Persentase Isotop 3 = 100%
x + 20 + y = 100
x + y = 100 – 20
x + y = 80
x = 80 - y
2580 - 34 tahun = 80-y
30
2580 – 34y = 30. (80 tahun)
2580- 34 tahun = 2400 - 30 tahun
2580 – 2400 = 34th-30y
4 tahun = 180
y = 80
4
y = 45%
4HAI Langkah: hitung nilai persentase x dalam ekspresi yang dibangun pada langkah ketiga.
x + y = 80
x + 45 = 80
x = 80 - 45
x = 35%
Oleh Saya Diogo Lopes Dias
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
HARI, Diogo Lopes. "Perhitungan massa atom"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/quimica/calculo-massa-atomica.htm. Diakses pada 27 Juni 2021.