HAI menghitung jumlah partikel atom digunakan untuk menunjukkan jumlah proton (dalam inti), elektron (dalam elektrosfer) dan neutron (dalam inti) yang ada dalam atom atau ion apa pun. Untuk melakukan ini, penting untuk mengetahui beberapa karakteristik atom:
1- Nomor atom (Z)
Ini adalah kode matematika, diwakili oleh huruf kapital Z, diposisikan di sisi kiri bawah singkatan atom:
ZX
Ini menunjukkan jumlah proton (p) dalam nukleus dan jumlah elektron (e) di elektrosfer atom. Jadi, secara umum:
Z = p = e
2- Nomor massa (A)
Ini adalah kode matematika yang sesuai dengan jumlah jumlah proton (p) dan neutron (n), keduanya ada dalam inti atom apa pun. Persamaan yang mewakili nomor massa diberikan oleh:
A = p + n
Karena jumlah proton sama dengan nomor atom, kita dapat menulis persamaan untuk menghitung nomor massa sebagai berikut:
A = Z + n
Jika kita mengetahui nomor massa dan nomor atom suatu atom, kita dapat menentukan jumlah neutron sebagai berikut:
n = A - Z
3- ion
Mereka adalah atom yang kehilangan atau mendapatkan elektron. Mereka memiliki tanda positif atau negatif yang diposisikan di kanan atas representasi mereka, seperti pada model berikut:
X+ atau X-
Ion positif: Ini disebut kation dan tanda positif menunjukkan bahwa ia telah kehilangan elektron.
Ion negatif: Ini disebut anion dan tanda negatif menunjukkan bahwa ia telah memperoleh elektron.
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
4- Kemiripan atom
a) Isotop
Atom-atom yang memiliki nomor atom sama dan nomor massa berbeda. Contoh:
7X14 dan 7kamu16
Atom X dan Y memiliki nomor atom yang sama (di sebelah kiri akronim), yaitu sama dengan 7. Atom X memiliki nomor massa (di sebelah kanan akronim) sama dengan 14, dan atom Y memiliki nomor massa sama dengan 16.
b) isobar
Atom-atom yang memiliki nomor massa sama dan nomor atom berbeda. Contoh:
15X31 dan 13kamu31
Atom X dan Y memiliki nomor massa (di sebelah kanan akronim) sama dengan 31. Atom X, di sisi lain, memiliki nomor atom sama dengan 15, dan atom Y memiliki nomor atom sama dengan 13.
c) Isoton
Atom-atom yang memiliki nomor massa dan nomor atom berbeda, tetapi jumlah neutronnya sama.
d) Isoelektronika
Atom-atom yang memiliki jumlah elektron yang sama. Contoh:
12X+2 dan 7kamu-3
Atom X memiliki nomor atom sama dengan 12 dan merupakan kation (dengan muatan positif +2), sehingga kehilangan dua elektron, sehingga memiliki 10 elektron di elektrosfernya. Atom Y, di sisi lain, memiliki nomor atom sama dengan 7 dan merupakan anion (dengan muatan negatif -3), sehingga memperoleh tiga elektron, sehingga memiliki 10 elektron di elektrosfernya.
Peta Pikiran: Partikel Atom
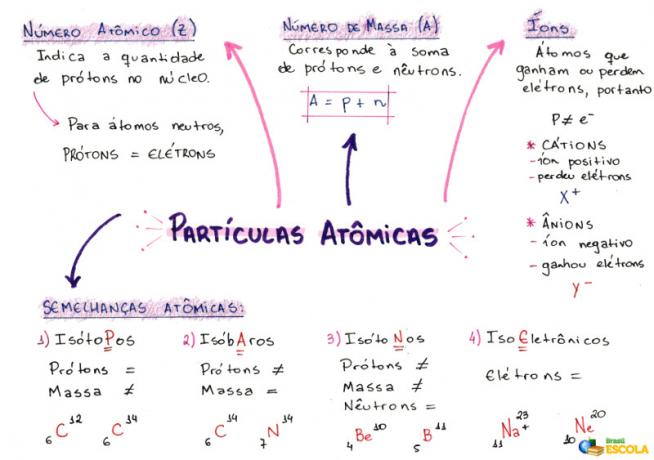
* Untuk mengunduh peta pikiran dalam PDF, Klik disini!
Contoh menghitung jumlah partikel atom
Contoh 1: Tentukan jumlah proton, neutron, dan elektron dalam atom 14X29.
Nilai berikut untuk atom X diberikan:
Nomor massa (kanan atas) = 29
Nomor atom (kiri bawah) = 14
Untuk menentukan jumlah proton:
Jumlah proton selalu sama dengan nomor atom, sehingga atom X memiliki 14 proton.
Untuk menentukan jumlah elektron:
Karena atom X bukan ion, maka jumlah elektron sama dengan jumlah proton, yaitu 14.
Untuk menentukan jumlah neutron:
Jumlah neutron ditentukan dengan menggunakan jumlah massa dan proton dalam rumus berikut:
A = p + n
29 = 14 + n
29 - 14 =n
n = 15
Contoh 2: Tentukan jumlah proton, neutron, dan elektron dari ion X+3, mengetahui bahwa nomor massa dan nomor atomnya berturut-turut adalah 51 dan 23.
Nilai berikut untuk ion X diberikan:
Nomor massa = 51
Nomor atom (kiri bawah) = 23
Untuk menentukan jumlah proton:
Jumlah proton selalu sama dengan nomor atom, sehingga atom X memiliki 23 proton.
Untuk menentukan jumlah elektron:
Ion X positif (+3), sehingga merupakan kation yang kehilangan tiga elektron. Jadi jumlah elektronnya adalah 20.
CATATAN: Pengurangan atau penambahan jumlah elektron selalu terjadi dalam kaitannya dengan nomor atom.
Untuk menentukan jumlah neutron:
Jumlah neutron ditentukan dengan menggunakan jumlah massa dan proton dalam rumus berikut:
A = p + n
51 = 23 + n
51 - 23 =n
n = 28
Contoh 3: Sebuah atom W memiliki nomor atom dan massa masing-masing sama dengan, 29 dan 57, isobare dari a atom Y, yang memiliki nomor atom sama dengan 30, yang merupakan isotop dari atom B, yang nomor massanya adalah 65. Dengan informasi ini, tentukan jumlah proton, neutron, dan elektron dalam atom B.
Data yang disediakan oleh latihan:
Atom W
nomor atom (kiri bawah) = 29
nomor massa (kanan atas) = 57
Y isobar, yaitu massa Y juga 57.
atom Y
nomor atom = 30
nomor massa = 57
Dengan dua nilai ini, kita harus menentukan nomor neutronnya karena merupakan isoton dari unsur B:
A = Z + n
57 = 30 + n
57 - 30 = n
n = 27
atom B:
nomor massa = 65
jumlah neutron = 27
Dengan data ini, kita harus menentukan nomor atomnya, karena dengan itu, kita akan menentukan jumlah proton dan jumlah elektronnya (karena bukan ion):
A = Z + n
65 = Z +27
65 - 27 = Z
Z = 38
Oleh karena itu, atom B memiliki 38 proton, 38 elektron, dan 27 neutron.
* Peta Pikiran oleh Victor Ricardo Ferreira
guru kimia
Oleh Saya Diogo Lopes Dias


