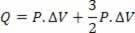Dalam proses isovolumetrik, volume tetap konstan dan karena itu tidak ada kerja yang dilakukan. Pertukaran panas dengan medium sama dengan perubahan energi internal sistem (lihat grafik di atas).
Menurut Hukum Pertama Termodinamika, dalam setiap proses termodinamika jumlah panas Q diterima oleh suatu sistem sama dengan kerja yang dilakukan oleh sistem ditambah variasi energi internalnya. Oleh karena itu, persamaan yang mewakili hukum pertama berikut di bawah ini:
Q=τ+∆U
Seperti yang dinyatakan dalam paragraf pertama, di mana dikatakan bahwa tidak ada pekerjaan, kita harus τ=0. Jadi, kalor yang dipertukarkan dengan medium sama dengan peningkatan energi internal sistem. Dengan demikian, kami memiliki:
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
Q=∆U
Ketika panas disuplai ke sistem, yaitu, ketika Q positif, energi internal akan meningkat; dan ketika sistem kehilangan panas, yaitu, ketika Q negatif, energi internal akan berkurang. Proses volume konstan terjadi ketika wadah berisi bahan kaku (misalnya tabung gas).
Saat menerima panas, sistem cenderung memuai, tetapi terhalang oleh dinding bejana, sehingga tekanan dan suhu sistem meningkat.
Oleh Domitiano Marques
Lulus Fisika
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
SILVA, Domitiano Correa Marques da. "Hukum pertama untuk proses isovolumetrik"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/fisica/primeira-lei-para-processos-isovolumetricos.htm. Diakses pada 27 Juni 2021.