Általában a vizes elektrolízis és magmás elektrolízis grafit és platina elektródákkal hajtják végre, amelyek nem vesznek részt a reakcióban; csak elektromos áramot vezetnek. Vannak azonban olyan speciális esetek, amikor szükséges használni aktív elektródákazaz redukción és oxidáción mennek keresztül.
Ezen elektródok fő felhasználási esetei, amelyek részt vesznek a redox folyamatban, a következők: a elektrolitikus fémtisztításpéldául cink, kobalt, nikkel és különösen réz; és a galvanizálás. Lássuk, hogyan fordulnak elő az egyes esetek:
• Réz elektrolitikus tisztítás: ez az elektrolitikus rézfinomítás körülbelül 99,9% -os tisztaságot eredményezhet, és főleg előállítására használják rézhuzalok, amelyek, ha a legkevesebb szennyeződést tartalmazzák, nagyon elektromos áram vezetésére képesek csökkentett.
Figyelje meg, hogyan zajlik ez a folyamat, látva az alábbiakban összeállított elektrolitkád vázlatát:

Potenciálkülönbséget alkalmaznak a réz-szulfát vizes oldatára (CuSo4 (aq)) - amely villamos energiát vezet - így az anód, amely tisztátalan fémréz, elveszíti az elektronokat, vagyis oxidálódik, felszabadítja kationjait (Cu
2+), amelyek a negatív lemezre rakódnak le. Ez lehet egy inert platina lemez, vagy jobb, ha tiszta rézlemez. Ez alkotja a katódot, amely redukálódik, mivel a réz lerakódik benne. Így az elektródokban előforduló félreakciók a következők:Ne álljon meg most... A reklám után még több van;)
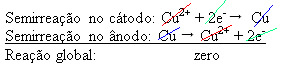
Az a tény, hogy nulla eredményt adott, azt jelzi, hogy nem volt kémiai reakció, csak a réz szállítása történt meg. A tartály alján találhatók a rézben lévő egyéb tisztátalan anyagok, mint például arany, ezüst, szilícium-dioxid (homok) és más ásványi anyagok, amelyek akár el is adhatók.
• Galvanizálás: fémbevonatot alkalmaznak egy olyan anyagra, amelyet védeni kell a korróziótól.
A bevonathoz választott fém - amely lehet króm (krómozás), nikkel (nikkelezés), ezüst (ezüstezés), arany (aranyozás) vagy cink (galvanizálás) - az anód, pozitív elektróda lesz, amely oxidáción megy keresztül, elektronokat veszít. A védett anyag helyett oxidálódik, mert redukciós potenciálja nagyobb.
A negatív elektród, vagyis a katód, amely ezeket az elektronokat befogadja és redukción megy keresztül, maga az az anyag, amelyet bevontak. Ily módon akkor is védett marad, ha a felületét valamilyen módon megsértik.
Írta: Jennifer Fogaça
Kémia szakon végzett
Hivatkozna erre a szövegre egy iskolai vagy tudományos munkában? Néz:
FOGAÇA, Jennifer Rocha Vargas. "Elektrolízis aktív elektródákkal"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/eletrolise-com-eletrodos-ativos.htm. Hozzáférés: 2021. június 28.


