Gázideál az, ahol a ütközések a részecskék között tökéletesen rugalmasak. Részecskéi között nincs semmiféle interakció, mint például erők vonzóak vagy visszataszítóak, ráadásul ezek a részecskék nem foglalnak helyet.
Szerint a a gázok kinetikai elmélete, az ideális gáz termodinamikai állapotát a nyomás, kötet és hőfok.
Nézis: Kalorimetria: gondolattérkép, képletek és megoldott gyakorlatok
ideális gázkoncepció
Az ideális gázok kizárólag részecskékban benméretekpontos (elhanyagolható méretű), amelyek vannak mozgalomkaotikus be van kapcsolva magassebesség. Ebben a típusú gázban a hőmérséklet és a részecskék transzlációs sebessége arányos.
Mivel az ideális gáz részecskéi között nincs kölcsönhatás, a belső energia ennek a gáznak mindig megegyezik a kinetikus energia az összes alkotó részecske közül.
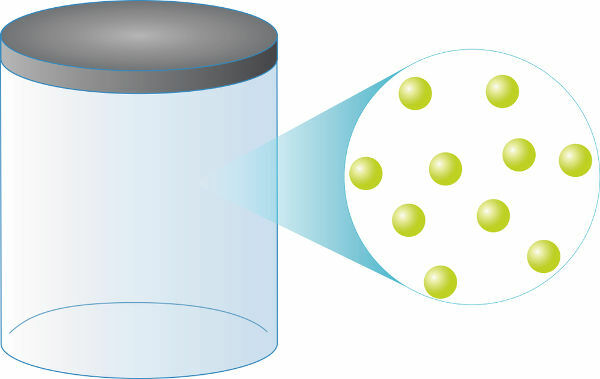
Bármi legyen is az ideális gáz, mindig ugyanaz lesz számban benrészecskék ugyanarra a kötetre. Tömegük viszont közvetlenül az önétől függ
moláris tömeg (g / mol-ban mérve), továbbá 1 mol ideális gáz (kb. 6.0.1023 részecskék) mindig elfoglalják a térfogata 22,4 l.Ön gázokigazi, ahol előfordul ütközésekrugalmatlan a részecskék között nagyon közel kerülnek az ideális gázok viselkedéséhez alacsony nyomású és magas hőmérsékletű rendszerek. Véletlen, hogy a Föld normál nyomás- és hőmérsékleti viszonyai között (25 ° C és 1 atm) a legtöbb a gázok ideális gázként viselkednek, és ez megkönnyíti a termodinamikai viselkedésre vonatkozó előrejelzések kiszámítását azok.
Néhány gáz, például a vízpára, amelyet a légköri gáz, nem tekinthető ideális gáznak, de igen gázokigazi. Ezeknek a gázoknak jelentős kölcsönhatása van részecskéik között, amelyek képesek sűríteni, ami őket okozza felenged, ha van ilyen hőmérséklet-csökkenés.
Az ideális gázok jellemzői
Nézze meg itt: absztrakt, az ideális gázok néhány jellemzője:
- Bennük csak tökéletesen rugalmas ütközések fordulnak elő a részecskék között;
- Bennük nincsenek kölcsönhatások a részecskék között;
- Bennük a részecskék elhanyagolható méretűek;
- 1 mol ideális gáz 22,4 l térfogatot foglal el, függetlenül attól, hogy mi a gáz;
- A valódi gázok ideális gázként viselkednek alacsony nyomáson és magas hőmérsékleten;
- A legtöbb gáz az ideális gázokhoz hasonlóan viselkedik.
ideális gáztörvény
A tudósok által kidolgozott gázok vizsgálata Károlyfiú,JózsefLouismeleg-lussac és Robertfiú megjelenéséhez vezetett három empirikus törvény, az ideális gázok viselkedésének magyarázatára használják a hőfok, nyomás és hangerőállandók, illetőleg.
Ezek a törvények együttesen képezték a szükséges alapot a ideális gáztörvény, amely a a gáz kezdeti termodinamikai állapota, amelyet a P mennyiségek határoznak meg1, T1 és V1, Te valamiddel végső termodinamikai állapot (P2, V2 és T2), miután szenvedtek néhányat gáztranszformáció.
Nézze meg a képlet általános gáztörvény
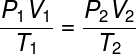
Az általános gáztörvény kimondja, hogy az termék ad nyomás szőrme hangerőnak,-nekgáz, osztva a termodinamikai hőmérséklettel, kelvinben egyenlő egy állandóval. Ezt az állandót viszont a clapeyron-egyenlet, néz:
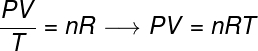
nem - anyajegyek száma (mol)
R - tökéletes gázok univerzális állandója (0,082 atm.l / mol. K vagy 8,31 J / mol. K)
A képletben P a gáz által kifejtett nyomás, V a gáz által elfoglalt térfogat, és T a hőmérséklet kelvinben mérve. a nagyság nem az anyajegyek számára utal, míg R az ideális gázok univerzális állandója, amelyet gyakran atm.l / mol egységekben mérnek. K vagy J / mol. K, utóbbit a SI.
Nézis:Mi a napszél és hogyan befolyásolja a Föld légkörét?
Ideális gáz belső energiája
A energiabelső az ideális gázok kiszámítható a állandóban benBoltzmann és a termodinamikai hőmérséklet, vegye figyelembe:
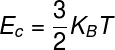
KB - Boltzmann-állandó (KB = 1,38.10-23 J / K)
Az előző kapcsolatból, amely lehetővé teszi számunkra a átlagos kinetikus energia az ideális gáz részecskéiből a következő képletet rajzoljuk le, amely alapján kiszámítható, hogy mi a a molekulák átlagos négyzetsebessége ideális gáz adott T hőmérsékletre, vegye figyelembe:
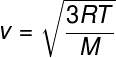
M - moláris tömeg (g / mol)
Ezzel a képlettel láthatja, hogy a kiegészítésnál nélhőfok ideális gáz a részecskék átlagos négyzetsebességének növekedését eredményezi.
Többet tud:Tudja meg, miből áll a fény és milyen jellemzői vannak
Megoldott gyakorlatok ideális gázokra
1. kérdés) Két mol ideális gáz és 1 atm nyomáson található 227 ° C hőmérsékleten. Számítsa ki literben a gáz által elfoglalt térfogatot.
Adat: R = 0,082 atm.l / mol. K
a) 75 l
b) 82 l
c) 15 liter
d) 27 liter
e) 25 l
Sablon: B betű
Felbontás:
Ennek a gáznak a térfogatának kiszámításához a Clapeyron-egyenletet használjuk, azonban a számítás megkezdése előtt a 227 ° C hőmérsékletet kelvinné kell átalakítani. Ehhez ehhez a hőmérséklethez hozzáadjuk a 273-as faktort, ami 500 K hőmérsékletet eredményez.
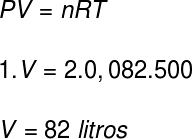
Az állásfoglalás szerint a gáz által elfoglalt térfogat 82 liter.
2. kérdés) Az ideális gáz 20 liter térfogatot foglal el, ha 3 atm nyomásnak van kitéve, így hőmérséklete állandó marad, miközben térfogata megháromszorozódik. Számítsa ki ennek a gáznak a végső nyomását, miután átesett ezen az átalakuláson.
a) 1 atm
b) 3 atm
c) 5 atm
d) 8 atm
e) 9 atm
Sablon: A betű
Felbontás:
A gyakorlat megoldásához a gázok általános törvényét fogjuk használni, vegye figyelembe:
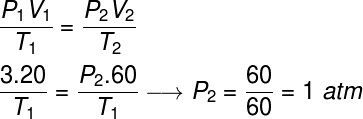
A számítás elvégzéséhez 60 liter térfogatot kellett rendelni a gázhoz, mivel térfogata az átalakulás során megháromszorozódott.
Rafael Hellerbrock
Fizikatanár
