Az elhatárolódás bázisok ez egy fizikai folyamat amely a szervetlen anyagok ezen fontos csoportjával fordul elő, ha vízben oldják őket, vagy amikor átmennek a fúziós folyamaton (átjutás a szilárd állapotból a folyékony állapotba keresztül fűtés).
Általában a jelenség alap disszociáció az alkotó kationok és anionok felszabadulása ionos vegyület, amely ebben az esetben az alap. Tehát a alap disszociáció, a ionok amelyek már léteznek a vegyületben, vagyis nem alakulnak ki új ionok.
A bázist bármilyen (X) fém képezheti, amely a vegyület kationja, vagy az ammónium kationt (NH csoport4+), kapcsolódva a hidroxid-anionhoz (amelyet az OH-csoport képvisel), az alábbi ábrák szerint:
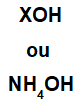
Az alapképlet általános ábrázolása
formája képviselik a alap disszociáció olyan egyenleten keresztül történik, amelyben a reagensben megvan a bázis, a termékekben pedig az ionok (kationok és anionok). A különbség az, hogy a disszociáció hogyan zajlik:
Az alap vízben való feloldása:
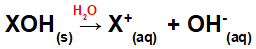
A bázis vizes közegben történő disszociációját ábrázoló egyenlet
Elhatárolódás alapösszevonással:
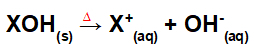
Egy bázis fúziós folyamat általi disszociációját képviselő egyenlet
A fenti általános egyenleteket elemezve ellenőrizzük, hogy mindegyikben mindig meg lesz-e az alapunk, a kation (ami a fém- vagy NH-csoport4+) és az anion (OH-). De vajon mind ilyenek? Nincs köztük különbség? Az első kérdésre a válasz nem, a második kérdésre a válasz igen.
Amikor elvégezzük a elhatárolódás egy bázistól, alapvető, hogy először elemezzük az alapképletet, mert ebből meg tudjuk határozni a kation és a hidroxid-anionok molmennyisége, mivel a kationmól-mennyisége standard (mindig 1 mol).
Érdemes megjegyezni, hogy a bázisképletben jelen lévő OH-csoportok mennyisége határozza meg a kation töltését és a hidroxid-anion mennyiségét a bázis disszociációjában.
Nézzük meg az alumínium-hidroxid példáit [Al (OH)3] és arany-hidroxid (AuOH). Az alumínium alap képletben három OH csoport, az arany alap képletben pedig csak egy OH csoport található. Így ezen alapok disszociációjában:
Al (OH) disszociáció3:
Mivel ennek a bázisnak három OH csoportja van a képletben, a kation töltése +3 lesz, és az anionok mennyisége molban egyenlő 3 mol, amint azt a következő egyenlet láthatja:
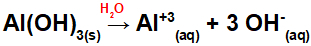
Alumínium bázis disszociációs egyenlet vizes közegben
Elhatárolódás az AuOH-tól:
Mivel ennek a bázisnak OH-csoportja van a képletben, a kation töltése +1 lesz, és az anionok mennyisége molban egyenlő 1 mol, amint azt a következő egyenletben láthatjuk:
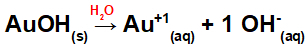
A bázis disszociációjának egyenlete vizes közegben lévő arannyal
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm
