Lorenzo Romano Amedeo Carlo Avogadro (1776-1856) olasz vegyész volt, aki először megalapozta azt az elképzelést, hogy Egy elem mintája, amelynek grammban kifejezett tömege numerikusan megegyezik az atomtömegével, mindig azonos számú atomot tartalmaz (N).
Maga Avogadro nem tudta meghatározni az N értékét. A huszadik század folyamán azonban a technológia és a tudományos ismeretek fejlődése lehetővé tette, hogy más tudósok technikákat dolgozzanak ki annak meghatározására. Amikor ezt az értéket végre felfedezték, hívták Avogadro állandója, ennek a tudósnak a tiszteletére, mivel ő volt az, aki megalapozta létrehozását.

Lorenzo Romano Amedeo Carlo Avogadro (1776-1856)
Bármely entitás (atomok, molekulák, elektronok, képletek vagy ionok) 1 móljában pontosan benne van az Avogadro-állandó értéke.
Az alábbi táblázat néhány értéket mutat az Avogadro konstansra vonatkozóan, amelyet a 20. század során kaptunk:
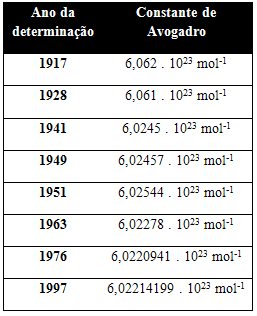
Az alábbiakban bemutatunk néhány technikát, amelyekkel megpróbálják meghatározni Avogadro állandójának értékét:
Az első tudós, aki hozzávetőlegesen kiszámította Avogadro állandóját, Johann Joseph Loschmidt volt. 1867-ben a gázok kinetikai elméletére alapozta és meghatározta, hogy hány molekula létezik 1 cm-ben3 egy gáz.
Ezen tudósok egyike a francia Jean Baptiste Perrin (1870-1942) volt, aki egy szuszpenzióban megszámolta az egységnyi térfogatú kolloid részecskék számát és megmérte azok tömegét. A talált érték 6,5 és 7,2 között volt. 1023 egységek mol. Ez a tudós 1913-ban kiadta a könyvet Les Atomes (1. kiadás Paris: Alcan), és 1924-ben kiadott 9. kiadása 16 módszert tartalmazott Avogadro állandójának kísérleti megszerzésére.

Jean Baptiste Perrin (1870-1942)
Évekkel később James Dewar (1842-1923) tudós Bertram Boltwood (1870-1927) radiokémikus és Ernest fizikus által évekkel korábban kidolgozott módszert használt. Rutherford (1871-1937), amely alapvetően abból állt, hogy megszámolták a radioaktív forrás által kibocsátott alfa részecskéket és meghatározták a kapott hélium gáz térfogatát. A Dewar által talált érték 6,04 volt. 1023 mol-1.
Még a 20. században Robert Millikan (1868-1953) kísérletet végzett az elektron töltésének meghatározására (1.6. 10-19 Ç). Mivel 1 mól elektron töltése már ismert volt (96500 C), ezt a két értéket össze lehetett kapcsolni, és a következő értéket lehetett megtalálni Avogadro állandójához: 6,03. 1023 mol-1.
Jelenleg az Avogadro konstans ajánlott értéke 6,02214 x 1023 mol-1 és ezt röntgendiffrakció útján határozzuk meg, amelynek során néhány kristályos rács atomjának térfogatát kapjuk, feltéve, hogy a mintában 1 mol atom sűrűsége és tömege ismert.
Didaktikai célokra a középiskolában, ahol a számításoknak nem kell olyan pontosaknak lenniük, mint a vegyi laboratóriumokban, az Avogadro állandóját 6,02. 1023 mol-1.
Vannak egyszerűbb módszerek is, amelyek segítségével a hallgatók meghatározhatják Avogadro állandóját a gyakorlatban. Az egyik elektrolízissel történik vizes közegben.
Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/determinacao-constante-avogadro.htm
