A mindennapi életben és a laboratóriumokban vannak olyan reakciók és átalakulások, amelyek spontánok, mások pedig nem spontán. Például minden égés spontán reakció, mert miután elindult, addig folytatódik, amíg az összes üzemanyag el nem fogy, vagy amíg az összes oxigén el nem fogy.
Másrészt az elektrolízis nem spontán folyamat, amelynek során az elektromos energia kémiai energiává alakul. Ilyen például a nátrium-klorid (NaCl) elektrolízise. Ha ezen az olvadt són elektromos áramot vezetünk, redoxireakciók és fémes nátrium (Nas) és klórgáz (Cl2. g)). Ha abbahagyjuk az elektromos áram működtetését, a reakció nem folytatódik önmagában, ami azt mutatja, hogy ez nem spontán.
A reakció spontaneitása a Gibbs-Helmholtz-egyenlet, lásd lejjebb:

Mire:
∆G = a szabad energia változása;
∆H = entalpia változás;
T = hőmérséklet Kelvinben (mindig pozitív);
∆S = entrópiaváltozás.
Ez az egyenlet azért kapta a nevét, mert J. amerikai fizikus javasolta. Willard Gibbs (1839-1903) és Hermann Helmholtz német fizikus (1821-1894).
Annak érdekében, hogy jobban megértsük, hogyan segít ez az egyenlet meghatározni a reakció spontaneitását, nézzük át röviden az egyes benne szereplő fogalmakat:
- ∆H (entalpia variáció): Az entalpia (H) egy anyag energiatartalma. Eddig semmilyen módon nem lehet meghatározni. A gyakorlatban az érhető el, ha egy folyamat entalpia-variációját (∆H) kaloriméterek segítségével mérjük. Ez a variáció a a folyamat során felszabadult vagy elnyelt energia.
- ∆S (entrópia variáció):Az entrópia (S) az a termodinamikai mennyiség, amely a rendellenesség mértékét méri.
Például az olvadó jégben a molekulák szilárd állapotból folyékony állapotba kerülnek, ahol nagyobb a dezorganizáció. Ez azt jelenti, hogy ebben a folyamatban az entrópia megnőtt (∆S> 0).
Az ammónia (NH3), 1 mol nitrogéngáz reagál 3 mol hidrogéngázzal (azaz 4 mol molekula van a reagensekben), így 2 mol ammónia keletkezik:
N2. g) +3 H2. g) → 2 NH3. g)
Mivel ebben a folyamatban a gázfázisban lévő molekulák száma csökken, a dezorganizáció csökkent, ami azt jelenti, hogy az entrópia is csökkent (∆S <0).
- ∆G (szabad energia): Szabad energia ill Gibbs szabad energia (mert csak ez a tudós javasolta 1878-ban) az a munka hasznosítására szolgáló rendszer hasznos energiája.
Egy rendszernek globális energiája van, de ennek az energiának csak a töredékét használják fel munkára, ezt Gibbs-mentes energiának hívják, amelyet a G.
Gibbs szerint egy folyamat akkor tekinthető spontánnak, ha munkát végez, vagyis ha G csökken. Ebben az esetben az átalakítás végső állapota stabilabb lesz, mint a kezdeti, amikor ∆G <0.
Ez alapján a következőket vonhatjuk le:

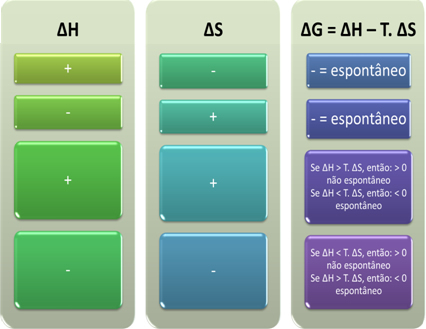
Azt is megnézhetjük, hogy egy folyamat spontán lesz-e, ha megnézzük a ibH és elmS algebrai előjelét a Gibbs-Helmholtz-egyenletben:
Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/energia-livre-gibbs.htm