A hibridizációs elmélet a Oktet elmélet, sikerült megmagyarázni nagyobb számú molekula szerkezetét, beleértve a bór által alkotott molekulákat is (B).
Ennek az elemnek öt alapállapotú elektronja van, a következő elektronikus konfigurációval:
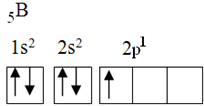
Az oktett elmélet szerint a bór csak egy kovalens kötést tud létrehozni, mivel csak egy hiányos atompályája van. Kísérletileg azonban meg kell jegyezni, hogy ez az elem olyan vegyületeket képez, amelyekben egynél több kötést végez.
Ilyen például a bór-trifluorid (BF3). Amint az alábbiakban látható, a bór három kovalens kötést hoz létre a fluorral, három pár kettő megosztásával elektronok és az utolsó héjában (valensréteg) hat elektron van, azaz kivétel a oktett.
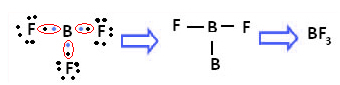
Ezt a bórnál előforduló hibridizációs jelenség magyarázza. Kiderült, hogy a 2. alszint elektronja elnyeli az energiát, és gerjesztett állapotba kerül, amelyben a 2p alszint üres pályájára ugrik. Ily módon három hiányos pálya képződik, amelyek most három kovalens kötést hozhatnak létre:
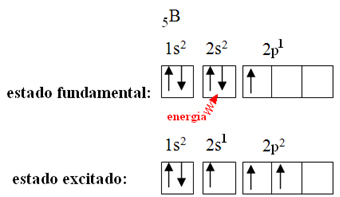
A bór-trifluoridban képződött kötések azonban azonosak, de ha fentebb nézzük, két kötés van különböző, mivel az egyiket egy s, a másik kettőt pedig egy ilyen típusú pályával készítenék. típus o. Itt zajlik le a hibridizáció, vagyis a hiányos pályák összeolvadnak, így hármat eredményeznek
hibrid pályák vagy hibridizált, amelyek azonosak és különböznek az eredetitől: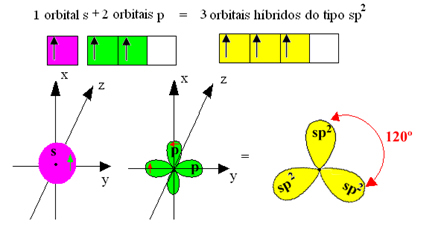
Mivel ezek a hibrid pályák egy s orbitálból és két p pályából állnak, ezt a hibridizációt nevezzük sp² hibridizáció.
A bórhoz kötődő fluornak kilenc elektronja van. Elektronikus terjesztése és pályái az alábbiakban láthatók:
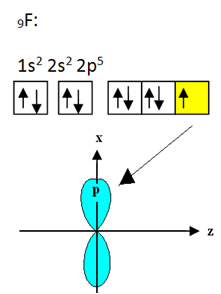
Megjegyezzük, hogy minden fluoratom csak egy kovalens kötést képes létrehozni, és hogy az ezt a kötést létrehozó pálya p típusú. Tehát az alábbiakban figyelje meg, hogyan alakulnak ki a pályák, amikor a BF-t alkotó kapcsolatokat hozzuk létre3 és nézze meg, hogy a hivatkozások milyenek σp-sp2:
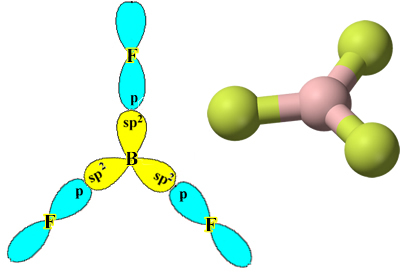
Ez más elemekkel is megtörténik, lásd például a „Berillium hibridizáció”.
Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/hibridizacao-boro.htm



