A víz önmagában nem tudja eltávolítani a zsírt az anyagokból. Ez azért van, mert Aa víz sarki, amint azt az alábbi kép mutatja, molekuláik hidrogén- és oxigénatomjai között fennálló elektronegativitásbeli különbség miatt. Másrészről, a zsír nem poláros és ezért a víz nem oldja fel a zsírokat.
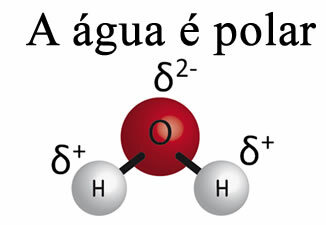
Ezenkívül a víznek van valami ún felszínes feszültség. Ezt jobban meg tudja érteni a szövegben. A víz felületi feszültsége, de alapvetően egyfajta rugalmas film vagy membrán képződik a víz felszínén, amely megakadályozza, hogy a szövetekbe és más anyagokba behatoljon a szennyeződések eltávolítása érdekében. A vízmolekulák minden irányba vonzzák egymást hidrogénkötések, de a felszíni molekulák csak az oldalán és az alatta lévő molekulákkal lépnek kölcsönhatásba, ezzel különbséget hozva létre kohéziós erők, ami a felszíni molekulák összehúzódását és ezen felületi feszültség kialakulását okozza.
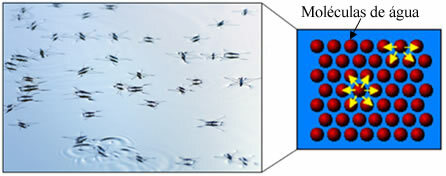
Ott jönnek be a szappanok és a mosószerek (latinul méregtelenít = tiszta), amelyeket szintén nevezünk felületaktív anyagok
, mivel képesek csökkenteni a víz felületi feszültségét, és emellett kölcsönhatásba lépnek mind a vízzel, mind a zsírral. Hogyan történik ez?A szappanok és detergensek zsírsav-sókat tartalmaznak, amelyek hosszú molekulák, amelyeket a nem poláris rész (mi a hidrofób – hidro = víz; fóbák = idegenkedés) és a sarki vég (hidrofil – hidro = víz; phyla = barát). Az alábbiakban a szappan tipikus felépítése van:
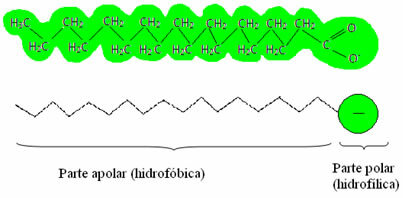
A mosószerek általában hosszú láncú szulfonsavak sói:
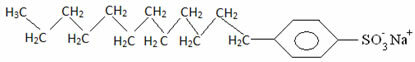
Így ezeknek a molekuláknak a szappanokban és detergensekben lévő nem poláris része kölcsönhatásba lép a zsírral, míg a sarki vég kölcsönhatásba lép a vízzel, kis gömbökbe csoportosulva, hívott micellák, amelyben a hidrofil részek a micella külsejével néznek szembe a vízmolekulákkal érintkezve, és a a zsír belül marad, érintkezve a nem poláros vagy hidrofób részével, a képen látható folyamathoz hasonló folyamat a kövesse:
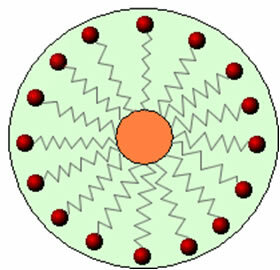
Ily módon a zsíros szennyeződés beszorul a micellák közepébe, és eltávolítható. Egy másik szempont, hogy a mosószerek és a szappanok képesek csökkenteni a víz felületi feszültségét, mert csökkenti a molekulák közötti kölcsönhatásokat, ezáltal megkönnyítve a különböző anyagok behatolását a piszok.
Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/quimica-dos-saboes-detergentes.htm
