A enyhe oxidáció alkénekben egy szerves reakció, amelyet adott esetben hajtanak végre alkén vizet és kálium-permanganát sót (KMnO4), só, amelyet általában neveznek Bayer reagens.
A képződött terméket ún alkohol vicinális, vagyis két hidroxilcsoportot tartalmazó alkoholok (OH-) a szomszédos szénatomokra helyezve, az alábbi általános képlet szerint:
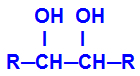
JEGYZET: R lehet gyökök vagy hidrogénatom.
Bayer Reagens
Amikor az Bayer reagens (KMnO4) szervetlen bázis (OH.) jelenlétében vízzel keverjük-) reakcióba lép és kálium-oxidot képez (K2O), mangán-dioxid (MnO2) és a kialakulóban lévő oxigének (szabad oxigén, amelyet [O] képvisel). Lásd a folyamat kiegyensúlyozott egyenletét.

Ezek a Bayer-reagensből képződő, kialakulóban lévő oxigének felelősek az enyhe oxidációs reakcióért az alkénekben (amint azt a következő tételekből láthatjuk).
Mechanizmusok enyhe oxidációs reakcióban alkénekben
1. mechanizmus: kialakulóban lévő oxigének képződése Bayer reagenséből;
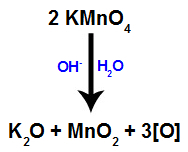
2. mechanizmus: A kialakulóban lévő oxigének támadása az alkénben jelenlévő kettős kötéshez, ami a pi kötés és ennek következtében szabad vegyérték kialakulása az egyes szénatomokban pi link.
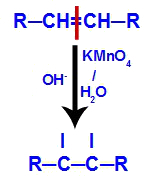
3. mechanizmus: A kialakuló oxigének egyesülnek a hidroniumokkal (H+), amely a víz önionizálásából képződik, és hidroxilcsoportokat eredményez (OH-).
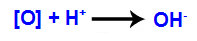
4. mechanizmus: A pi-kötést tartalmazó szénatomok mindegyikében lévő szabad vegyértékekben képződött hidroxilok összekapcsolódása egy vicinális alkoholalkoholból származik.

Példák enyhe oxidációs reakciókra alkénekben
→ Enyhe oxidációs reakció but-2-énen
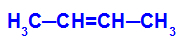
A but-2-én szerkezeti képlete
Kezdetben az alkén 2. és 3. szénatomja közötti kettős kötést a kialakuló oxigének támadása szakítja meg, szabad vegyértéket (függőleges nyomot) létrehozva a 2. és 3. szénatomon.

A 2. és 3. szénatom közötti pi-kötés megszakítása a but-2-énben
Ezután a kialakulóban lévő oxigén egyesül egy hidroniummal (H+) a víz ionizálásából hidroxilcsoportokat képezve (OH-), amelyek a 2. és 3. szén szabad vegyértékeihez kötődnek, ami vicinális dialkolt eredményez.
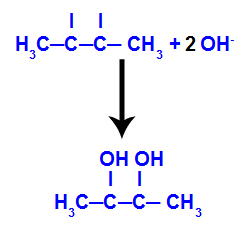
But-2-énből képződött vicinális alkohol
→ Enyhe oxidációs reakció 2-metil-propénon
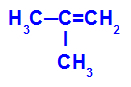
A 2-metil-propén szerkezeti képlete
Kezdetben az alkén 1. és 2. szénatomja közötti kettős kötést a kialakuló oxigének támadása bontja meg, szabad vegyértéket (függőleges nyomot) létrehozva az 1. és 2. szénatomon.
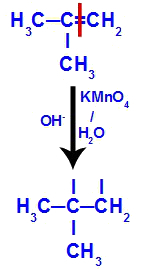
Az 1. és 2. szénatom közötti pi-kötés megszakítása 2-metil-propénben
Ezután a kialakulóban lévő oxigén egyesül egy hidroniummal (H+) a víz ionizálásából hidroxilcsoportokat képezve (OH-), amelyek az 1. és 2. szén szabad vegyértékeihez kötődnek, ami vicinális dialkolt eredményez.
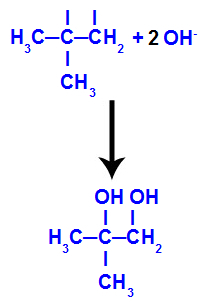
2-metil-propénből képzett vicin alkohol
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/oxidacao-branda-alcenos.htm


