A hassium, Hs és szimbólummal atomszám 108, a transzaktinidákként ismert elemek egyike. Mint ennek a csoportnak minden eleme, ez sem található meg a természetben, mivel szintetikus, amellett, hogy radioaktív és instabil. Szintézisét a Helmholtz Center for Heavy Ions Research (GSI) németországi laboratóriumának tulajdonítják. a németországi Darmstadium, és a nevét a németországi Hesse állam tiszteletére adták, amely a németországi középső régióban található. szülők.
A Hassium a legnehezebb elem, amelynek tulajdonságait maga a GSI végzett kísérletekkel elemezték. Az eredmények fontosak voltak a H-k helyzetének megerősítéséhez Periódusos táblázat, mivel ez az elem, valamint az ozmium és a ruténium, a 8. csoport könnyebb elemei közötti hasonlóságot észlelték.
Olvasd el te is:Bohrium – a Niels Bohrról elnevezett szintetikus kémiai elem
Hassium összefoglaló
Ez egy szintetikus kémiai elem, amely a periódusos rendszer 8. csoportjában található.
A németországi Darmstadiumban található Gesellschaft für Schwerionenforschung (GSI) szintetizálta.
Ez egy radioaktív elem és instabil.
Elméleti és kísérleti adatok megerősítik, hogy tulajdonságai hasonlítanak csoportja legkönnyebb elemeire.
Transaktinidként nem állítható elő nagy mennyiségben, kivéve néhány sebességgel. atomok.
Hassium tulajdonságai
Szimbólum: hs
Atomszám: 108
Atomtömeg: 277 c.u.
Elektronikus konfiguráció: [Rn] 7s2 5f14 6d6
A legstabilabb izotóp: 269Hs (14 másodperces felezési idő)
Kémiai sorozat: 8. csoport; transzaktinidek; szuper nehéz elemek.
Hassium jellemzői
A Hassium a szintetikus elem és a 8-as csoport legnehezebbje. Úgy tartják, a transzaktinid, éppen azért, mert az aktinida sorozat után megjelenik a periódusos rendszerben. Mint minden transzaktinid, a hassium is egy elem radioaktív és instabil.
Ez azt jelenti, hogy izotópjai elérik kevés ideje fél élet (az az idő, ami ahhoz szükséges, hogy az atomfajták tömege a felére csökkenjen). Jelenleg a haszium hét izotópja ismert, amelyek tömege 264 a.m.u és 270 a.m.u között változik. Az összes közül a legstabilabb az izotóp 269Hs, felezési ideje 14 másodperc.
Bár a rövid felezési idő megnehezíti a transzaktinidák kémiai tulajdonságainak tanulmányozását, a hassiumnak e tekintetben valamivel több szerencséje volt. 2001 júniusában bejelentették, hogy ő lett a legnehezebb elem, amelynek tulajdonságait elemezni kell.
Egy csapatnak sikerült a németországi Darmstádio városában körülbelül hat Hs atomot előállítania körülbelül 10 másodperces felezési idővel. Bár kevésnek tűnik, ez elég volt annak megerősítésére, hogy a haszium-oxid, a HsO4, erős hasonlóságot mutat a 8. csoport könnyebb elemeinek oxidjaival, a RuO-val4 és OsO4, ez a ruténium ez a ozmium.
Lásd még: Seaborgium - egy másik szintetikus kémiai elem, radioaktív tulajdonságokkal és rövid felezési idővel
Hassium megszerzése
A transzaktinidák közös jellemzője, hogy nehéz előállítani. Általában a legkorszerűbb berendezésekre van szükség, mint pl részecskegyorsítók. Ezekben az ionos fajok magas elemekkel ütköznek atomtömeg a szupernehéz elemek kialakításához (amelyben Hs is szerepel).
A hassium esetében a periódusos rendszer 8. csoportjában elfoglalt helyét megerősítő tanulmányok a magnézium-26 bombázásával, a kúrium-248 célpontjaként történő előállításával foglalkoztak.
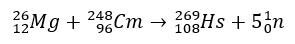
Az ezen elemek bevonásával végzett kísérletek költségesek, ezért gyakori, hogy elméleti vizsgálatokat végeznek, pontosan a kémiai tulajdonságok kiszámítására és előrejelzésére. A rövid felezési idő egy másik bonyolító tényező.
A kísérleti technikák szétválasztás és észlelés nagyon gyorsnak kell lennie a hiteles eredmények eléréséhez. Végül ezeknek az elemeknek a reakcióhatékonysága nagyon alacsony, néhány atomegység tartományba esik.
Óvintézkedések a Hassiummal
A H-t nem állítják elő nagy mennyiségben, ezért manipulálják nem jár kockázatokkal. Ezen túlmenően, erősen ellenőrzött környezettel rendelkező kutatóközpontokban szerzik be.
a hassium története

A transzaktinidák egy tudományos vita főszereplői voltak a Hidegháború, a Átigazolások háborúja, ez a név a fermium (Fm, Z = 100) utáni elemek előállításával és felismerésével kapcsolatos vitákra hivatkozva született. Ebben a versenyben a laboratóriumok vettek részt:
Közös Nukleáris Kutatóintézet, Dubna városában, Oroszországban;
Lawrence Berkeley Nemzeti Laboratórium a kaliforniai Berkeleyben;
Gesellschaft für Schwerionenforschung (GSI, jobban fordítva: Helmholtz Center for Research on Heavy Ions) a németországi Darmstadiumban.
A 108-as elem esetében a GSI és a Dubna csoport érintett. Bár a dubnai tudósok (Juri Oganessian vezetésével) először jelentették a 108-as elem jelenlétét, a német csoport tagjai vállalták az elismerést, mivel a GSI meggyőzőbb eredményeket mutatott be, míg az egyik kísérletben a 265-ös izotóp három atomját, míg egy másikban a 264-es izotóp egy atomját sikerült előállítania.
Ezeket az izotópokat az univerzális lineáris gyorsító (Unilac, jobb fordításban univerzális lineáris gyorsító) segítségével állították elő, az izotópok bombázásával. 208Pb by 58Hit. A Tiszta és Alkalmazott Kémia Nemzetközi Uniója (IUPAC) 1997-ben ismerte el a 108-as elemet, amelynek szimbóluma Hs. Hassium a német Hesse állam tiszteletére.
Hassziumon megoldott gyakorlatok
1. kérdés
A Hassium, a Hs szimbólum, a legnehezebb elem, amelynek tulajdonságait kísérletileg vizsgálták. Abban az időben a kutatók meg tudták határozni a hasium-tetroxid (HsO) tulajdonságait4. Ebben a fajban a Hs ugyanolyan NOx-ot tartalmaz, mint csoportjának könnyebb elemei, az ozmium (Os) és a ruténium (Ru). A Hs oxidációs száma a hasium-tetroxidban egyenlő:
a) 0
B) +2
C) +4
D) +6
E) +8
Felbontás:
Alternatív E
A oxigén, amikor a oxid, -2-vel egyenlő töltést kap. Így a NOx A Hs, amelyet x-nek nevezünk, a következőképpen számítható ki:
x + 4(-2) = 0
x - 8 = 0
x = +8
2. kérdés
A hassium legstabilabb izotópjának, a Hs-nek a felezési ideje mindössze 14 másodperc. Azt jelenti:
A) 14 másodperc alatt a Hs izotóp tömege megkétszereződik.
B) 14 másodperc elteltével a Hs izotóp tömege kisebb lesz, mint a kezdeti tömeg fele.
C) alig egy perc múlva a Hs izotóp tömege a kezdeti tömegének 1/16-a lesz.
D) egy perc múlva a Hs izotóp tömege pontosan a fele lesz a kezdeti tömegének.
E) 14 másodperc alatt a Hs izotóp tömege el lesz osztva 4-gyel.
Felbontás:
Alternatív C
A felezési idő azt az időt jelzi, amely szükséges ahhoz, hogy az atomfajták mennyisége felére csökkenjen. Ez azt jelenti, hogy 14 másodpercenként a felére csökken a Hs mennyisége. Ennek a felezési időnek a megfigyelésével egyértelmű, hogy 56 másodperccel már négy felezési időt értünk el, aminek következtében a H tömege 2-vel osztódik4, ami a 16.
Írta: Stefano Araújo Novais
Kémia tanár

