A szulfátok olyan ionos vegyületek, amelyek az SO aniont tartalmazzák42-, amelyet szulfátanionnak hívnak.
A kén a 16 vagy a VI-A család egyik eleme, ami azt jelenti, hogy vegyértékes héjában 6 elektron van. Az oktett szabály szerint további 2 elektron befogadására lenne szükség ahhoz, hogy az utolsó elektronhéjban 8 elektron legyen, és ezáltal stabil legyen. De a kén oktett terjeszkedésen megy keresztül, mivel a táblázat harmadik periódusában található elem Periodikus, viszonylag nagy, ami lehetővé teszi, hogy nyolcnál több elektron befogadására képes körül.
Így, amint az alább látható, a kén vegyértékszintje összesen 12 elektron befogadására bővül. De két oxigénatom még mindig nem stabil, mindegyik hét elektronvalenssel rendelkezik a vegyértékhéjban, ezért a stabilizáláshoz még egy elektronra van szükségük. Emiatt a két atom töltése -1, ami az anion teljes töltését eredményezi -2:
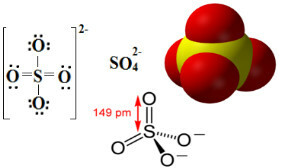
A szulfátanion származhat kénsavból (H2CSAK4 (aq)) lásd lent:
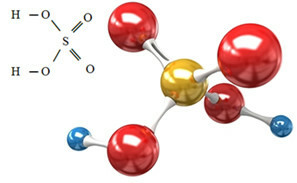
A kénsav valamilyen bázissal semlegesítő reakcióban reagál, szervetlen sót képezve, amely a mi szulfátunk, valamint vízzel:
Általános reakció: Kénsav + bázis → Só (szulfát) + víz
H2CSAK4 + 2 Çó →Ç2CSAK4+ 2 H2O
Lásd az alábbi példát, ahol kálium-szulfát képződik:
H2CSAK4 + 2 KOH →K2CSAK4+ 2 H2O
Vegye figyelembe, hogy a szulfát nómenklatúráját egyszerűen a következő szabály hajtja végre: szulfát + a hozzá kapcsolódó elem neve. Ezenkívül a szulfátokra vonatkozó képleteket úgy állítják elő, hogy az egyes ionok töltését kicserélik az elemindexre, és az "1" indexet nem kell írni:
Példák:
Nál nél+1 CSAK42- → Nál nél2CSAK4→ nátrium-szulfát
mg+2 CSAK42- → MgSO44→ magnézium szulfát
Itt+2 CSAK42- → Ügy4→ kalcium-szulfát
Ba+2 CSAK42- → BASO4→ bárium-szulfát
Al+3 CSAK42- → Al2(CSAK4)3→ alumínium-szulfát
A szulfátiont tartalmazó sók általában vízben oldódnak, a négy kivétel: kalcium-szulfát (CaSO4), stroncium-szulfát (SrSO4), bárium-szulfát (BaSO4) és ólom-szulfát (PbSO4). Ez azért van, mert nagy a kötési energia ezek között a kationok között (Ca2+uram2+, Ba2+ és Pb2+) és a szulfát, mivel mindegyiknek +2 töltete van, a szulfátanionnak pedig -2 töltése van. Így a kapcsolat megszakítása nehezebbé válik.
A szulfátok kristályrácsok formájában találhatók, az ellentétes töltések egymásra gyakorolt vonzása miatt, amint az alábbiakban látható a réz-szulfát esetében (CuSO4):

A szulfátok a természetben főleg ásványok formájában találhatók. Néhány példa:
barit → bárium-szulfát;
Gipsz → kalcium-szulfát;
Celestite → stroncium-szulfát;
anglesirendben → ólom-szulfát;
Glauberite → kettős kalcium- és nátrium-szulfát: CaNa2(CSAK4)2;
Kálium-alumínium (kalinit) → hidratált kettős kálium-alumínium-szulfát: KAl (SO42,11H2O
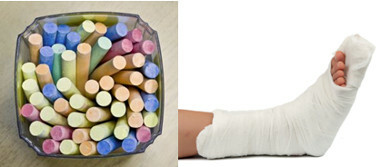
A mindennapi életben a fő szulfátok között van kalcium-szulfát, amelyet vízmentes formában (víz nélkül) az iskolai kréta gyártásához használnak. Ha dihidrát formában van, (CaSO4 .2h2O), gipsz néven ismert és bőségesebb. Hevítéskor kalcium-szulfát-hemihidrátot (CaSO4. ½H2O), amely gipsz, amelyet ortopédiában, fogászati formákban, polgári építőiparban és festékekben használnak.
Egy másik fontos só az smagnézium-szulfát (MgSO44), s néven ismertkeserű al vagy Epsom só, amely hashajtó hatású, masszázshoz és relaxáló fürdőkhöz használják.
Írta: Jennifer Fogaça
Kémia szakon végzett


